Srdeční selhání – statiny ve světle studie CORONA
Heart failure – statins in the light of the CORONA study
Statins are nowadays routinely recommended for prescription in ischemic heart disease. Whether they also improve the prognosis of patients with heart failure of ischemic origin is not yet known. We present a summary of the potential positive and negative effects of statins in patients with heart failure and subsequently analyse the results of the CORONA study. Although the results of this study did not prove a reduction in mortality as a result of treatment using rosuvastatin, there was a significant reduction in the number of hospitalizations from overall cardiovascular causes and from more severe heart failure. Given its minimal undesirable side effects and the improvement in the quality of life, further studies of the use of statins in heart failure would be desirable.
Key words:
statins – heart failure – CORONA study
Autoři:
J. Vítovec 1,2; J. Špinar 1,2
Působiště autorů:
I. interní kardioangiologická klinika LF MU
1; FN u sv. Anny v Brně
2
Vyšlo v časopise:
Kardiol Rev Int Med 2008, 10(3): 119-122
Souhrn
Statiny jsou dnes doporučovány jako rutinní součást léčby ischemické choroby srdeční, zda zlepšují i prognózu nemocných se srdečním selháním ischemické etiologie však není známo. Podáváme přehled možných příznivých i nepříznivých účinků statinů u nemocných se srdečním selháním a následně jsou rozebrány výsledky studie CORONA. Výsledky této studie sice neprokázaly snížení mortality při léčbě rosuvastatinem, ale významně se snížil počet hospitalizací jak pro celkové kardiovaskulární příčiny, tak pro zhoršené srdeční selhání. Vzhledem k minimálním nežádoucím účinkům rosuvastatinu a zlepšení kvality života jsou další studie se statiny u srdečního selhání žádoucí.
Klíčová slova:
Statiny – srdeční selhání – studie CORONA
Úvod
Příznivý vliv statinů – inhibitorů hydroxymetylglutaryl koenzym A reduktázy – na snížení úmrtnosti nemocných s vysokým kardiovaskulárním rizikem byl poprvé prokázán dvojitě slepou mortalitní studií 4S [20] a poté řada dalších studií u nemocných s ischemickou chorobou srdeční nebo zvýšeným kardiovaskulárním rizikem a různou plazmatickou hladinou cholesterolu prokázala stejný vliv na pokles úmrtnosti [19]. Příznivé účinky statinů jsou nejen ve snížení celkového a LDL cholesterolu, ale také v řadě možných nelipidemických vlivů [18]. U nemocných se srdečním selháním je popsána řada příznivých, ale také některých nepříznivých účinků, které se tak mohou rozdílně podílet na výsledcích klinických studií. Příznivá působení statinů u srdečního selhání spočívají v řadě reakcí od protizánětlivých, antioxidačních až po antiarytmické působení [16].
Protizánětlivé účinky
Je známo, že u srdečního selhání je aktivována celková zánětlivá reakce s aktivací prozánětlivých cytokinů, adhezivních molekul a komplementu C. To vše vede ke zhoršení prognózy nemocných se srdečním selháním [21]. Menšími studiemi je prokázáno, že statiny tyto prozánětlivé faktory potlačují a tím mohou příznivě průběh onemocnění ovlivnit [17].
Antioxidační účinky
Řada experimentálních i klinických studií naznačuje souvislost mezi zvýšením oxidativního stresu a stupněm srdečního selhání [6]. Statiny inhibují NADPH oxidázu s následným snížením oxidativního zatížení buněk myokardu a prevencí progrese srdeční hypertrofie [9, 11].
Endoteliální funkce
Je prokázán vztah mezi srdečním selháním a poruchou endoteliální funkce se snížením produkce vazodilatačního oxidu dusného (NO) a následnou poruchou cévní relaxace, zvýšené agregace destiček a aktivací proliferace hladkých svalových buněk [10]. Statiny zvyšují produkci endoteliální NO syntetázy se zvýšením vazodilatace po hyperemii a zlepšením srdeční funkce [22].
Srdeční hypertrofie, remodelace myokardu a neurohumorální aktivace
Srdeční selhání vede ke kompenzační a později nepříznivé srdeční hypertrofii. Zvýšení obsahu kolagenu a neurohumorální aktivace vede k srdeční remodelaci, zvýšení koncentrace angiotenzinu III a katecholaminů a tím ke zhoršení prognózy nemocných [12].
V experimentu statiny všechny tyto procesy zmírňují, a tak přispívají k částečnému zlepšení srdečního selhání [14].
Autonomní regulace a antiarytmický vliv
Srdeční dysfunkce vede k autonomní dysregulaci a následným poruchám srdečního rytmu. Zde opět statiny mají příznivý vliv na potlačení sympatické aktivity, snížení výskytu fibrilace síní a komorových arytmií [2].
Nesmíme však při hypotéze o příznivých účincích statinů u nemocných se srdečním selháním opomenout také možné nepříznivé vlivy na srdeční funkci:
Hypotéza endotoxin-lipoproteinová
Cholesterol a lipoproteiny bohaté na triglyceridy detoxikují bakteriální lipopolysacharidy (endotoxiny), které uvolňují zánětlivé cytokininy u srdečního selhání. Statiny zde mohou zvyšovat hladiny endotoxinů snížením hladiny lipidů a zhoršit srdeční funkci [16].
Hypotéza ubiquinonová
Statiny inhibují tvorbu ubiquinonu (koenzym Q10), který má centrální roli v řetězci mitochondriální respirace. Dochází ke snížení tvorby adenosin trifosfátu (adenosine triphosphate - ATP), nižší ochraně buněčné stěny proti volným kyslíkovým radikálům a ke zhoršení srdeční funkce [3].
Hypotéza selenoproteinová
Selenoproteiny hrají důležitou roli ve svalovém metabolizmu (kosterním i srdečním). Jejich dysfunkce spolu s deficitem selenu bývají spojeny s rozvojem myopatií. Statiny snižují aktivaci selenocysteinové RNA transferázy s redukcí selenoproteinu a tím mohou vyvolávat myopatie [13].
Podávání statinů u nemocných s chronickým srdečním selháním (ChSS), zvláště s hraničními hodnotami cholesterolu, je proto stále předmětem diskuzí [4, 5, 15]. Základem je skutečnost, že v mnohých studiích se statiny, byli nemocní se srdečním selháním vyřazováni, akutní koronární příhody nebyly časté a statiny byly považovány za rizikové léky pro srdeční selhání. Nízké hladiny cholesterolu jsou spojeny s horší prognózou nemocných se srdečním selháním, snížením hladin lipoproteinů může docházet k vyššímu vstupu enterálních endotoxinů do cirkulace a dalšímu zhoršení funkce levé komory a také se uvažuje o úloze snížené syntézy koenzymu Q10. Na druhé straně víme, že snížením reinfarktů pomocí statinů zlepšíme prognózu nemocných se srdečním selháním. I výskyt srdečního selhání ve studiích se statiny poklesl [15]. Při retrospektivní analýze klinických studií se srdečním selháním, a to jak ischemické, tak i neischemické etiologie, jsou výsledky rozporuplné [1, 4].
Proto se autoři studie CORONA rozhodli uspořádat první velkou dvojitě slepou studii, která si dala za cíl zjistit, jaký vliv má léčba statiny u nemocných se srdečním selháním [7].
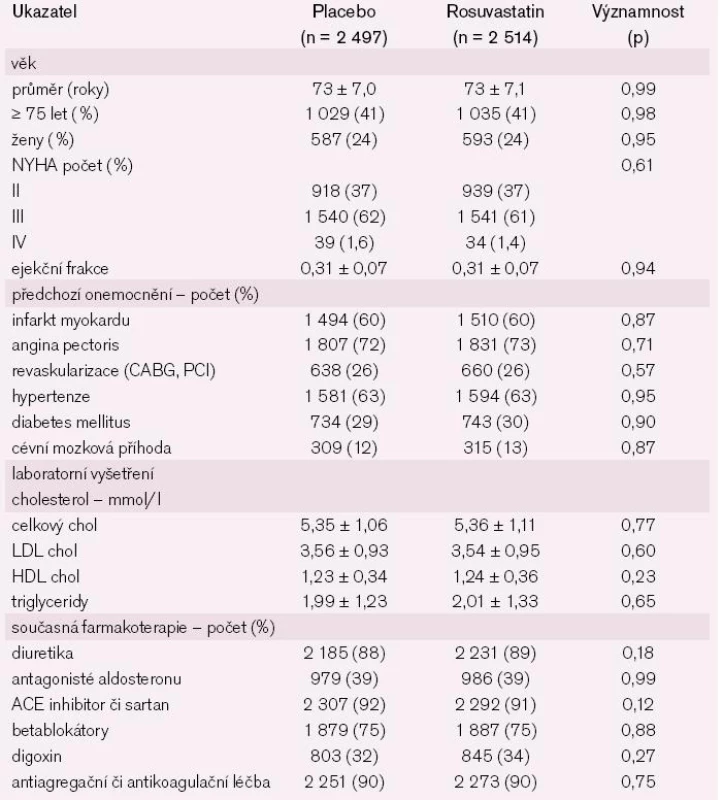
Do studie bylo zařazeno 5 011 pacientů starších 60 let s projevy srdečního selhání, ejekční frakcí pod 40 % a byla užita funkční klasifikace NYHA II–IV na podkladě prokázané ischemické choroby srdeční. Nemocní byli randomizováni na léčbu 10 mg rosuvastatinu nebo placeba. Primární cíl byl složený – úmrtí z kardiovaskulárních příčin, nefatální infarkt myokardu nebo nefatální CMP. Sekundární cíle zahrnovaly jakákoliv úmrtí, koronární příhody a hospitalizace. Charakteristika nemocných je uvedena v tab. 1.
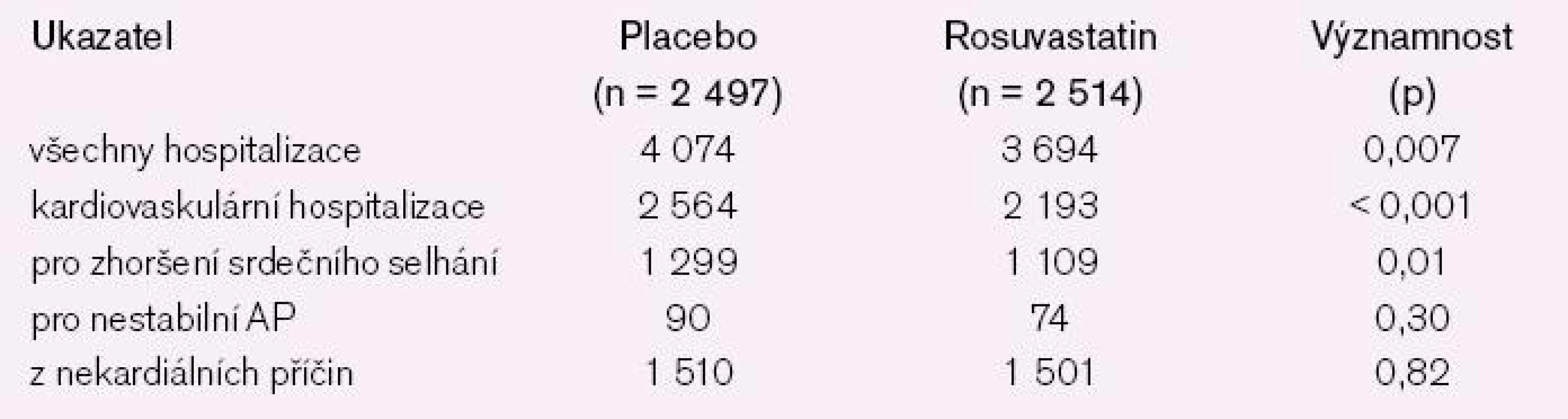
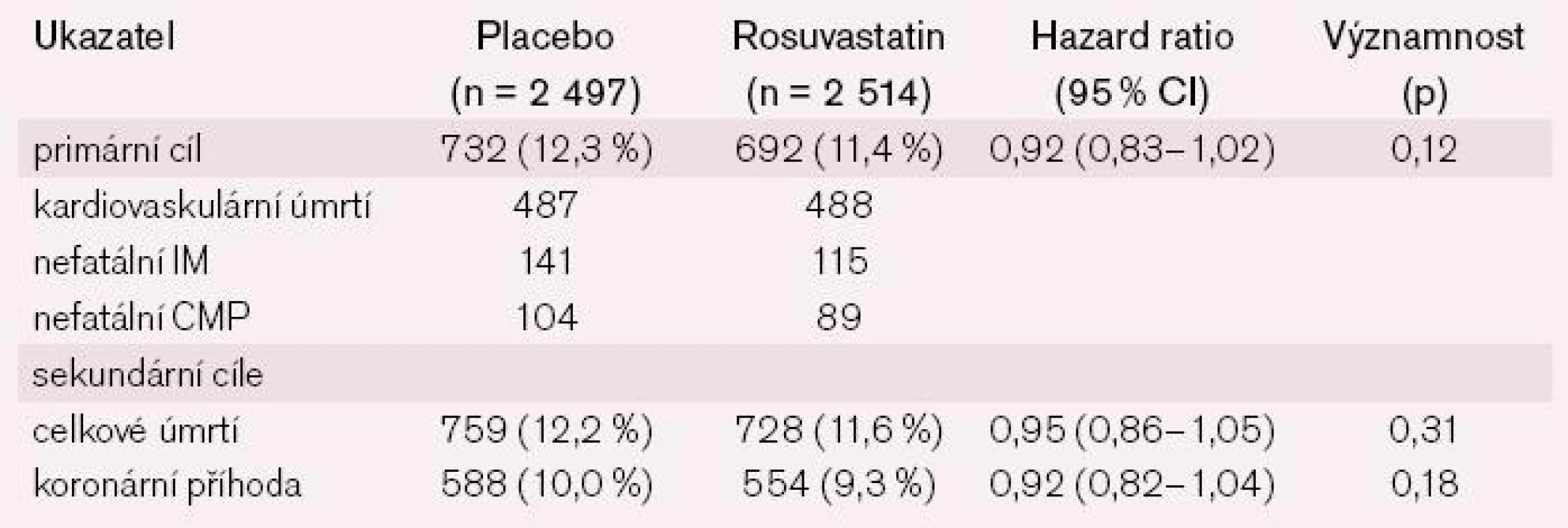
Dle předpokladu, ve skupině s rosuvastatinem byl významný pokles LDL cholesterolu z 3,54 na 1,96 mmol/l a triglyceridů z 2,01 na 1,56 mmol/l (obojí p < 0.001) oproti placebu, kde změny těchto ukazatelů nebyly pozorovány. Během mediánu sledování, tj. 32.8 měsíců se kombinovaný primární cíl vyskytl u 692 nemocných s rosuvastatinem a 732 na placebu (HR 0.92; 95 % CI, 0.83 to 1.02; p = 0.12) (graf 1). Ve výskytu úmrtí nebyl rozdíl; ve skupině léčené rosuvastatinem zemřelo 728 (28,9 %) nemocných a v placebové 759 (30,3 %) (HR, 0.95; 95 % CI, 0.86 to 1.05; p = 0.31). Nebyl také rozdíl ve výskytu koronárních příhod či kardiovaskulárního úmrtí (tab. 2). Ze sekundárních cílů byl významný pokles hospitalizací z kardiovaskulárních příčin u nemocných s rosuvastatinem (2 193) oproti placebu (2 564) (p < 0.001) a pokles nefatálních infarktů myokardu či cévních mozkových příhod (p = 0,05) (graf 2).


Důležité je, že bezpečnostní profil rosuvastatinu byl lepší než profil placeba: jak z hlediska přerušení podávání léčiva (placebo vs. rosuvastatin: 546 vs. 490), tak co do četnosti nepříznivých celkových účinků (302 vs. 241), gastrointestinálních (223 vs. 171) či neurologických (272 vs. 247). Nezávažné svalové bolesti byly více po statinu (144 vs. 167), stejně jako jakékoliv svalové symptomy (207 vs. 225). Autoři hodnotí bezpečnost rosuvastatinu srovnatelnou s placebem [8].
Závěr
Pokud si uvědomíme přínos pro zlepšení výsledků kvality života u nemocných se srdečním selháním a to, že rosuvastatin nezpůsobil zhoršení, ale spíše zlepšení míry nepříznivých případů i při vysazení léků, byla CORONA z hlediska kladených požadavků na kvalitu života pozitivní studie. Jistě, při přísném posouzení stran úmrtnosti přínos rosuvastatinu nebyl výrazný, a většinou ne moc významný, ale naznačený trend sleduje správný směr. Je velice pravděpodobné, že i přes neexistující formálně schválenou indikaci srdečního selhání, se právě díky přínosu a bezpečnostním hlediskům rozšíří používání rosuvastatinu u kompenzovaných nemocných se srdečním selháním a ICHS. Je zde řada podnětů, ze kterých se můžeme na základě studie CORONA poučit. Pokud vezmeme v úvahu výsledky jiných pilotních studií se statiny u srdečního selhání [1, 15] a vynikající bezpečnostní profil rosuvastatinu, mohly by se v budoucích randomizovaných studiích se srdečním selháním testovat vyšší dávky statinů i přesto, že ve studii CORONA s rosuvastatinem v nízké dávce 10 mg/den bylo významné snížení LDL cholesterolu či C-reaktivního proteinu [8]. Na základě časového vývoje výsledků studie CORONA a zejména stratifikace opožděné křivky úmrtnosti jsou další následné studie dobře ospravedlnitelné a bezpečné. V neposlední řadě by měly být sledovány realistické cíle kvality života s přiměřenými přínosy zvláště u starších nemocných se srdečním selháním. Pokud je lék skutečně bezpečný a má zřejmý klinický přínos, pak klasický kombinovaný konečný cíl zahrnující kardiovaskulární úmrtí, nefatální IM a mozkové příhody nemusí být o nic významnější než souborný výsledek zaměřený na kvalitu života.
Práce byla vypracována v rámci Výzkumného záměru MŠMT – MSM0021622402.
prof. MUDr. Jiří Vítovec, CSc., FESC
prof. MUDr. Jindřich Špinar, CSc., FESC
I. interní kardioangiologická klinika LF MU
a FN u sv. Anny v Brně
jiri.vitovec@fnusa.cz
Zdroje
1. Anker SD, Clark AL, Winkler R et al. Statin use and survival in patients with chronic heart failure: results from two observational studies with 5.200 patients. Int J Cardiol 2006; 112: 234–342.
2. Hanna IR, Heeke B, Bush H et al. Lipid-lowering drug use is associated with reduced prevalence of atrial fibrillation in patients with left ventricular systolic dysfunction. Heart Rhythm 2006; 3: 881–886.
3. Hargreaves IP. Ubiquinone: cholesterol’s reclusive cousin. Ann Clin Biochem 2003; 40: 207–218.
4. Hradec J. Má význam podávání statinů u nemocných se srdečním selháním? Interní Med 2008; 10: 216–218.
5. Hradec J. Klinická studie CORONA. Remedia 2005; 15: 169–171.
6. Keith M, Geranmayegan A, Sole MJ et al. Increased oxidative stress in patients with congestive heart failure. J Am Coll Cardiol 1998; 31: 1352–1356.
7. Kjekshus J, Dunselman P, Blideskog M et al. A statin in the treatment of heart failure? Controlled rosuvastatin multinational study in heart failure (CORONA): study design and baseline characteristics. Eur J Heart Fail 2005; 7: 1059–1691.
8. Kjekshus J, Apetrei E, Barrios V et al. Rosuvastatin in older patients with systolic heart failure. N Engl J Med 2007; 357: 2248-2261.
9. Krum H, Tonkin A. The Rosuvastatin Impact on Ventricular Remodeling, Cytokines and Neurohormones (UNIVERSE) Study (abstr). J Am Coll Cardiol 2006; 47: 61A–2A.
10. Landmesser U, Spiekermann S, Dikalov S et al. Vascular oxidative stress and endothelial dysfunction in patients with chronic heart failure: role of xanthine-oxidase and extracellular superoxide dismutase. Circulation 2002; 106: 3073–3078.
11. Maack C, Kartes T, Kilter H et al. Oxygen free radical release in human failing myocardium is associated with increased activity of rac1-GTPase and represents a target for statin treatment. Circulation 2003; 108: 1567–1574.
12. Mann DL. Mechanisms and models in heart failure: A combinatorial approach. Circulation 1999; 100: 999–1008.
13. Moosmann B, Behl C. Selenoprotein synthesis and side-effects of statins. Lancet 2004; 363: 892–894.
14. Nickenig G, Bäumer AT, Temur Y et al. Statin-sensitive dysregulated AT1 receptor function and density in hypercholesterolemic men. Circulation 1999; 100: 2131–2134.
15. Ramasubbu K, Estep J, White DL et al. Experimental and clinical basis for the use of statins in kardiol with ischemic and nonischemic cardiomyopathy. J Am Coll kardiol 2008; 5: 415–426.
16. Rauchhaus M, Coats AJ, Anker SD. The endotoxin-lipoprotein hypothesis. Lancet 2000; 356: 930–933.
17. Sola S, Mir MQ, Lerakis S et al. Atorvastatin improves left ventricular systolic function and serum markers of inflammation in nonischemic heart failure. J Am Coll Cardiol 2006; 47: 332–337.
18. Soška V. Farmakologie hyperlipoproteinémií. Vnitr Lek 2000; 46: 565–568.
19. Špinar J. et al. Klinické studie v kardiologii. Grada Publishing 2001.
20. Randomised trial of cholesterol lowering in 4,444 patients with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S). Lancet 1994; 344: 1383–1389.
21. Torre-Amione G, Kapadia S, Benedict C et al. Proinflammatory cytokine levels in patients with depressed left ventricular ejection fraction: a report from the Studies of Left Ventricular Dysfunction (SOLVD). J Am Coll Cardiol 1996; 27: 1201–1206.
22. Tousoulis D, Antoniades C, Vassiliadou C et al. Effects of combined administration of low dose atorvastatin and vitamin E on inflammatory markers and endothelial function in patients with heart failure. Eur J Heart Fail 2005; 7: 1126–1132.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2008 Číslo 3
Nejčtenější v tomto čísle
- Srdeční selhání s normální ejekční frakcí
- Katetrizační ablace fibrilace síní
- Srovnání rozdílů mezi muži a ženami u akutního infarktu myokardu
- Aerobní kapacita u nemocných s ischemickou chorobou srdeční