Kam se ubírá současný vývoj léků ovlivňujících krevní srážení?
Where is a step in the current development of drugs that affect blood clotting?
An overview of new anticoagulants – direct thrombin inhibitor dabigatran and direct FXa inhibitors rivaroxaban and apixaban and their indications according to the new Guidelines of the 9th ACCP and professional Societies for the prevention of thromboembolic complications after orthopedic surgery, for the treatment of venous thrombosis and pulmonary embolism and for the prevention of stroke or systemic embolisation in patients with atrial fibrillation.
Keywords:
dabigatran – rivaroxaban – apixaban – atrial fibrillation – development of therapy
Autoři:
J. Kvasnička
Působiště autorů:
Trombotické centrum, ÚLBLD VFN v Praze
Vyšlo v časopise:
Kardiol Rev Int Med 2012, 14(2): 103-108
Souhrn
V článku je podán přehled o nových antikoagulanciích – přímém inhibitoru trombinu dabigatranu a přímých inhibitorů faktoru Xa rivaroxabanu a apixabanu a jejich indikací podle nového doporučení 9. ACCP a odborných společností při prevenci tromboembolických komplikací po ortopedických operacích, při léčbě žilní trombózy a plicní embolie a při prevenci iktu nebo systémové embolizace u nemocných s nevalvulární fibrilací síní.
Klíčová slova:
dabigatran – rivaroxaban – apixaban – fibrilace síní – vývoj léčby
Úvod
Léky snižující krevní srážení nazýváme antikoagulancii. Přes možné riziko krvácení patří v klinické medicíně stále k základním, široce používaným lékům. Krátkodobě (bolus nebo několik hodin) jsou antikoagulancia používána k udržení nesrážlivosti krve při použití mimotělního oběhu nebo hemodialýzy a během perkutánní koronární intervence (PCI), střednědobě (v délce 10–35 dní) při primární prevenci tromboembolické nemoci (TEN) v pooperačním období nebo u akutně interně nemocných, kteří jsou připoutáni na lůžko. Dlouhodobě (řadu měsíců a let) se pak antikoagulancia aplikují při prevenci TEN či potratů spojených s trombotickými komplikacemi u těhotných žen (zde jen po dobu těhotenství a šestinedělí), při léčbě žilního tromboembolizmu nebo plicní embolie, při tromboembolické plicní hypertenzi, po mechanické náhradě srdeční chlopně a také při prevenci ischemického iktu nebo systémové tromboembolické příhody u nemocných s nevalvulární fibrilací síní aj. Indikaci k léčbě antikoagulancii, výběr léku, jeho dávku, perioperační léčebný postup a doporučovanou délku léčby na podkladě dostupných údajů z kontrolovaných klinických studií komplexně opět shrnují nyní v pořadí již 9. doporučení ACCP (American College of Chest Physicians) publikovaná v únoru 2012 [1].
Obecně je účinek antikoagulancií zaměřen na inhibici tvorby trombinu v různých etapách koagulační kaskády nebo tyto léky jeho účinek inhibují přímo. V některých indikacích se antikoagulancia ještě kombinují s protidestičkovými léky, což sice zvyšuje jejich antitrombotický účinek, ale zároveň zvyšuje i možné riziko krvácení. Tyto léky můžeme podle jejich zaměření, způsobu výroby a způsobu inhibice koagulace dělit na čtyři skupiny léků, z nichž některá antikoagulancia z prvních dvou skupin jsou v klinické medicíně používána již více než 70 let:
- Hepariny (nefrakcionovaný standardní heparin a nízkomolekulární hepariny – zkratka LMWH z angl. low molecular weight heparin) a víceméně selektivně působící inhibitor aktivovaného faktoru Xa (FXa) syntetický pentasacharid fondaparinux (Arixtra®, Glaxo), aplikované injekčně i. v. nebo s. c.
- Kumarinové preparáty (antagonisté vitaminu K), používané per os, u nás je to nyní jen warfarin.
- Přímé přirozené inhibitory trombinu – hirudin a jemu podobné látky (např. bivalirudin), s injekční nebo perorální formou podání.
- Nové perorální přípravky povolené u nás k použití v posledních čtyřech letech – přímé inhibitory faktoru Xa – rivaroxaban (Xarelto®) a apixaban (Eliquis®) a přímý inhibitor trombinu dabigatran etexilát (Pradaxa®).
Účinek antikoagulancií v různých úsecích koagulační kaskády je znázorněn na obr. 1.
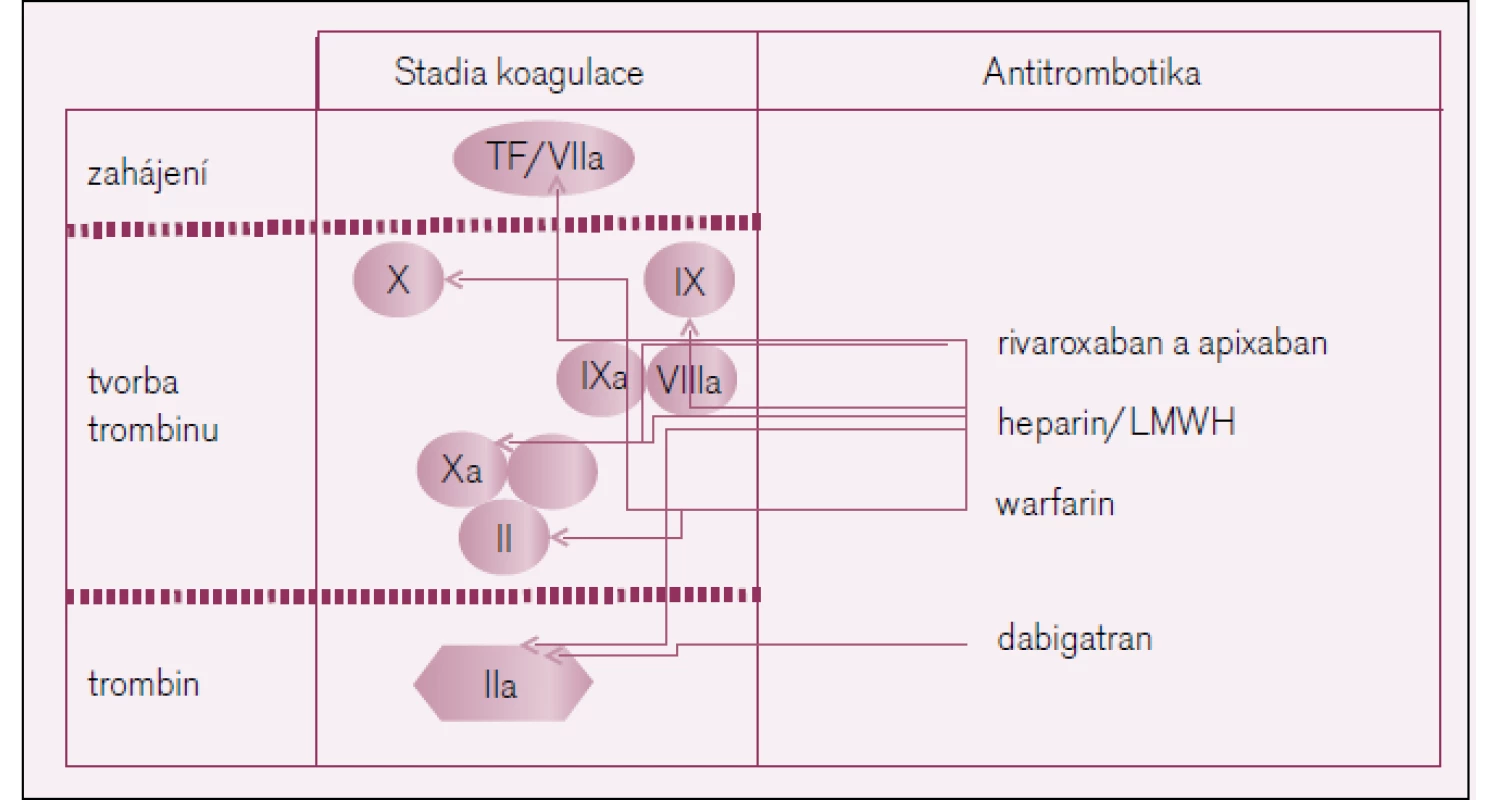
Léky v prvních dvou skupinách je možné označit za tzv. nepřímé inhibitory koagulačních faktorů, neboť ke svému antikoagulačnímu účinku potřebují buď kofaktor antitrombin (heparin, LMWH či pentasacharid), nebo v případě warfarinu indukují tvorbu neúčinných koagulačních faktorů (PIVKA – protein induced by vitamin K absence). Léky ve třetí a čtvrté skupině řadíme mezi přímé inhibitory koagulačních faktorů nebo trombinu, protože ke své aktivitě nepotřebují kofaktory a v místě koagulační kaskády působí selektivně.
Předpokládá se, že tato „nová“ antikoagulancia budou v budoucnu postupně nahrazovat ta „starší“ – hlavně z důvodů omezené výroby heparinů, které se stále vyrábějí ze zvířecí tkáně. Warfarin se zase řadu let umísťuje na prvním místě léků s nežádoucím účinkem a s komplikacemi vyžadujícími hospitalizaci, zejména u starších osob [2].
Přímé inhibitory F Xa
Rivaroxaban (Xarelto®, Bayer)
Tento přípravek je v ČR registrován od 30. 9. 2008. Jde o přímý selektivní inhibitor F Xa s rychlým nástupem účinku. Faktor Xa působí v katalýze konverze protrombinu na trombin. Aktivace faktoru Xa je společným bodem „vnitřní“ i „vnější“ cesty koagulační kaskády. Na rozdíl od trombinu není faktor Xa zapojen do antitrombotického systému směřujícího k aktivaci proteinu C a S. Jako optimální pro profylaktickou léčbu po ortopedických operacích totální náhrady kyčelního nebo kolenního kloubu byla ve studiích odvozena standardní dávka 10 mg 1krát denně. Na rozdíl od warfarinu není nutno dávkování měnit a upravovat podle laboratorního monitorování. Biologická dostupnost po orálním podání odpovídá 60–80 %. Zhruba 2/3 podaného množství látky podléhají metabolické přeměně v játrech za vzniku neaktivních metabolitů, zbylá 1/3 je vylučována ledvinami v aktivní formě. Kontraindikace jeho podání však nastává až při těžké poruše funkce ledvin (clearance kreatininu (CrCL) < 15 ml/min) nebo při závažné jaterní nedostatečnosti s koagulopatií a krvácením je možnost vzniku jeho vyšších krevních hladin a krvácení. Jinak lze lék s opatrností použít i při lehčích formách uvedených poruch, např. při hodnotách CrCL 15–30 ml/min, nebo u jaterní poruchy typu Child-Pugh B. Jeho indikace není omezena ani věkem či váhou nemocného. Rivaroxaban také nemá klinicky významnější interakce se současně podávanými léky, při použití protidestičkových léků je však třeba opatrnosti. Nevýhodou je neznalost antidota, při krvácení je třeba vyčkat, až jeho účinek pomine, poločas přípravku je 7–11 hod [3]. Pokud dojde ke krvácení, lze jej řešit jen symptomaticky, například mechanickou kompresí, chirurgickým zákrokem, náhradou tekutin a zajištěním hemodynamické podpory, transfuzí krve nebo krevních komponent (plazmy) [4]. Nově byly provedeny studie, které sice u zdravých osob nebo u myší po podání koncentrátu protrombinového komplexu dokázaly snížit navozené patologické hodnoty koagulačních testů (PT nebo APTT, TE-gramu) [5], ale krvácení nezabránily. V pokusu s myší k tomu nedošlo ani po podání rekombinantního aktivovaného F VII [6].
Při dodržování doporučeného dávkování nemusí být rivaroxaban při léčbě laboratorně kontrolován. Pokud je však třeba, lze k sledování ovlivnění koagulace použít protrombinový čas (PT), který je tímto lékem ovlivňován úměrně k dávce. Z reagencií je k provedení tohoto testu doporučován Neoplastin™ (Diagnostica Stago, Asnières, Francie), který ukazuje velmi dobrou korelaci mezi výsledky testu a plazmatickými koncentracemi rivaroxabanu (hodnota R je 0,98). Jiné reagenty mohou přinést jiné výsledky. Hodnotu PT je však bez kalibrátorů nutno odečíst během několika sekund, protože INR (mezinárodní normalizovaný poměr) je kalibrován a validován pouze pro kumariny a nelze jej s přiměřenou přesností využívat pro jiná antikoagulancia. Aktivita anti-faktoru Xa je sice rivaroxabanem ovlivněna také, ale žádný kalibrační standard opět není k dispozici [4].
Další nově schválenou indikací rivaroxabanu v Evropě (včetně ČR) a nyní patrně i FDA v USA je jeho podání při prevenci cévní mozkové příhody a systémové embolizace u dospělých pacientů s nevalvulární fibrilací síní s jedním nebo více rizikovými faktory, jako jsou městnavé srdeční selhání, hypertenze, věk 75 let a vyšší, diabetes mellitus, prodělaná cévní mozková příhoda nebo tranzitorní ischemická ataka. Vychází se zde z výsledků studie ROCKET-AF, která prokázala non-inferioritu rivaroxabanu v dávce 20 mg 1krát denně v porovnání s léčbou warfarinem (při intention-to-treat analýze), resp. superioritu rivaroxabanu (on-treatment analýza). Výskyt krvácivých komplikací byl celkově srovnatelný, méně závažná krvácení byla častější, a ta závažná, zejména intrakraniální, byla naopak méně častá [7].
Další u nás schválenou indikací rivaroxabanu je léčba hluboké žilní trombózy a prevence recidivující hluboké žilní trombózy a plicní embolie po akutní hluboké žilní trombóze u dospělých. Vychází se zde z výsledků studie EINSTEIN a ENSTEIN EXTENSION. U pacientů se závažnou formou hluboké žilní trombózy mělo 2,1 % (36 z 1 731) pacientů léčených rivaroxabanem buď recidivu hluboké žilní trombózy, nebo plicní embolii ve srovnání s 3 % (51 z 1 718) pacientů, kteří užívali antagonisty vitaminu K (při INR 2,0–3,0) [8].
Při léčbě plicní embolie se v nejnovější studii opět jasně ukázalo, že rivaroxaban nemá horší účinek než warfarin, resp. byla opět prokázána jeho non-inferiorita (p = 0,003). V rivaroxabanové studii došlo k 2,1% výskytu rekurence plicní embolie, u warfarinu v 1,8 % (hazard ratio = 1,12; 95% CI (0,75–1,68)). Rovněž bezpečnost rivaroxabanu zde byla statisticky vyhodnocena jako shodná (p = 0,23). Závažná krvácení se však ve skupině pacientů léčených rivaroxabanem vyskytovala méně často (1,1 % vs 2,2 %, p = 0,003) [8].
Dávkování rivaroxabanu je v obou indikacích vyšší než při profylaxi TEN v ortopedii.
Pokud se používá k prevenci mrtvice nebo systémové embolie u pacientů s nevalvulární fibrilací síní, činí doporučená dávka rivaroxabanu 20 mg jednou denně. Léčba tímto přípravkem by zde měla pokračovat za předpokladu, že její přínos převyšuje riziko krvácení. Tablety se užívají spolu s jídlem. Pokud se rivaroxaban používá k léčbě hluboké žilní trombózy nebo jejího opětovného výskytu a k léčbě plicní embolie, činí doporučená úvodní dávka 15 mg 2krát denně po dobu prvních tří týdnů, poté následuje dávka 20 mg jednou denně.
Rivaroxaban byl nyní také testován proti placebu při léčbě nemocných s akutním koronárním syndromem (studie ATLAS ACS 2 – TIMI 51) s délkou studie 12 týdnů, maximem až 31 měsíců. Všichni nemocní s rivaroxabanem (v dávce 2krát 2,5 mg nebo 2krát 5 mg denně) nebo s placebem dostávali současně protidestičkové léky aspirin a clopidogrel. Výsledky studie byly zveřejněny v lednu 2012. Úmrtí na rekurenci infarktu a z dalších kardiovaskulárních příčin nebo iktu ve skupině léčené rivaroxabanem byla proti placebu lehce snížena (hazard ratio 0,84, p = 0,008). V poklesu úmrtí na kardiovaskulární příhody však prospěla jen dávka 2krát 2,5 mg, vyšší dávka již úmrtnost nesnížila. Pravděpodobně proto, že po rivaroxabanu docházelo k vyššímu počtu závažných krvácení (2,1 % proti 0,6 %, p < 0,001) proti placebu, včetně intrakraniálních (0,6 % proti 0,2 %, p = 0,009). V konečném výskytu fatálních krvácení sice statistický rozdíl proti placebu nalezen nebyl, ale pokud byly porovnávány obě dávky rivaroxabanu mezi sebou, nižší dávka 2krát 2,5 mg měla i nižší výskyt fatálního krvácení než dávka 2krát 5 mg (0,1 % proti 0,4 %, p = 0,04) [9].
Obecně platí, že rivaroxaban nelze podávat těhotným ani dětem, resp. mladistvým pod 18 let. V této věkové skupině s ním nejsou žádné klinické zkušenosti.
Apixaban (Eliquis®, Bristol-Myers Squibb/Pfizer)
Jedná se o další vysoce selektivní reverzibilní inhibitor F Xa, který je nyní od 18. 5. 2011 registrovaný v ČR v indikaci prevence žilních tromboembolických příhod u dospělých pacientů, kteří podstoupili elektivní náhradu kyčelního nebo kolenního kloubu v dávce 2krát denně 2,5 mg [10]. Apixaban má malou molekulu s významným antitrombotickým efektem. Interakce s cytochromem P 450 je minimální. Biologický poločas má 10–14 hod, maximální koncentrace dosahuje po 3–4 hod, nemá žádnou interakci s jídlem. Není to „pro-drug“ a nemá aktivní metabolity. Je metabolizován více játry jako rivaroxaban, méně je vylučován ledvinami. Jeho kontraindikace jsou velmi podobné rivaroxabanu, zejména ve vztahu k jaterní nebo ledvinné dysfunkci. Pacienti se zvýšenými jaterními enzymy ALT/AST > 2krát norma laboratoře (ULN) nebo se zvýšeným celkovým bilirubinem ≥ 1,5krát ULN byli z klinických studií vyřazeni. Proto se apixaban musí v těchto případech podávat s opatrností. Před zahájením léčby je tedy třeba kontrola jaterních testů ALT. Podává se 2krát denně 2,5 mg, přičemž první dávka může být použita za 12–24 hod po operaci. Antidotum ani zde neexistuje. Předávkování apixabanem tedy může způsobit vyšší riziko krvácení. V případě výskytu hemoragických komplikací musí být léčba přerušena a zjištěn zdroj krvácení. Mělo by se zvážit zahájení vhodné léčby, např. chirurgická zástava krvácení nebo transfuze mražené plazmy. Rovněž podání živočišného uhlí.
V důsledku inhibice F Xa prodlužuje apixaban testy srážlivosti, jako jsou například protrombinový čas (PT), INR a aktivovaný parciální tromboplastinový čas (aPTT). Při očekávané léčebné dávce byly zaznamenány malé změny těchto testů srážení, které jsou také velmi variabilní. Tyto testy se tedy nedoporučují ke zhodnocení farmakodynamických účinků apixabanu. Apixaban však také vykazuje inhibici F Xa, která je zřejmá ze snížení enzymatické aktivity faktoru Xa v mnoha komerčních anti-F Xa soupravách. Výsledky mezi jednotlivými soupravami se ale mohou lišit.
Přípravek nelze opět podávat těhotným ani dětem, resp. mladistvým pod 18 let. V této věkové skupině nejsou s apixabanem žádné klinické zkušenosti [10]. Zdá se však, že půjde o relativně bezpečný přípravek, pokud bude podáván ve schválených indikacích. Proběhla s ním již celá řada studií v rámci klinického programu EXPANSE (60 tis. pacientů ve 45 zemích světa) a na základě dobrých výsledků apixabanu proti nízkomolekulárnímu heparinu enoxaparinu (studie ADVANCE 1–3) v ortopedii byla schválena i jeho nynější indikace. Další studií s kladným výsledkem pro apixaban je již dokončená studie The Apixaban for Reduction in Stroke and Other Thrombotic Events in Atrial Fibrillation (ARISTOTLE), kde byl porovnáván apixaban s warfarinem. Apixaban zde redukoval roční výskyt ischemického iktu nebo systémové embolizace o 21 % (1,27 % vs 1,6 % při warfarinizaci/1 rok, hazard ratio = 0,79; 95% CI, 0,66–0,95; p < 0,001). Apixaban byl u nemocných s nevalvulární fibrilací srdečních síní také výrazně lepší ve svém profylaktickém účinku než aspirin. Dle výsledků studie AVERROES (prevence iktu a embolie u pacientů s nevalvulární fibrilací síní, kde není indikován warfarin) bylo dosažené hazard ratio jen 0,45 (p < 0,001) [11]. Další zajímavé výsledky se nyní očekávají od studie zaměřené na léčbu hluboké žilní trombózy a plicní embolie AMPLIFY (první týden apixaban v dávce 2krát denně 10 mg, pak 2krát 5 mg denně), opět v porovnání s warfarinem, a také od pokračování této studie (AMPLIFY EXT) po 6–12 měsících, zde již jen proti placebu.
Nyní byly publikovány i výsledky studie APPRAISE-2 s dávkováním apixabanu 5 mg denně u nemocných s akutním koronárním syndromem. Ta však úspěšná nebyla. V porovnání s placebem nedošlo ani k redukci rekurence ischemických příhod a pro zvýšené riziko krvácení při léčbě apixabanem (hazard ratio 2,59) byla nakonec předčasně ukončena [12]. Zajímavé na ní bylo i to, že jen 44 % z pacientů s akutním koronárním syndromem mělo PCI, ostatní měli jen farmakologickou léčbu. Tedy velký rozdíl proti situaci v léčbě akutního koronárního syndromu v ČR.
Přímý inhibitor trombinu
Dabigatran etexilát (Pradaxa®, Boehringer--Ingelheim) je prvním novým antikoagulanciem, které bylo schváleno Evropskou komisí k léčebnému použití. Bylo to již 27. 3. 2008. Je v současnosti také jediným dostupným perorálním přímým reverzibilním inhibitorem trombinu na trhu. Jde o „pro-drug“ dabigatran etexilát, který je až v organizmu metabolizován na aktivní substanci dabigatran. Tato substance má rychlý nástup účinku (1–4 hod) s poměrně dlouhou dobou působení s poločasem 12–17 hod [13]. Přípravek se vyrábí v dávkování 75 mg, 110 mg a 150 mg. Nemá interakci zprostředkovanou izoenzymy cytochromu P450, proto jeho interakce s léky je minimální (mimo současné aplikace s verapamilem, amiodaronem, dronedaronem a chinidinem). Kontraindikací použití dabigatranu je mimo krvácivé stavy i porucha funkce jater nebo stav při jaterním onemocnění s očekávaným dopadem na přežití (je tedy nutno kontrolovat jaterní testy). Proto z léčby mají být vyloučeni pacienti, u kterých byly hodnoty jaterních enzymů zvýšeny nad dvojnásobek horní hranice normálních hodnot laboratoře. Dále je zde kontraindikací i souběžná léčba systémově podávaným ketokonazolem, cyklosporinem, itrakonazolem nebo takrolimem. Protože je tento přípravek převážně vylučován ledvinami (80 %), je třeba před zahájením léčby zhodnotit u každého pacienta funkci ledvin podle clearance kreatininu. Z léčby dabigatranem pak mají být vyloučeni všichni nemocní s těžkou poruchou ledvin s nálezem CrCL pod 30 ml/min. Tato kontrola CrCL by měla být i během léčby, zejména u nemocných, u kterých lze zhoršení ledvin očekávat (např. při hypovolemii, dehydrataci, při souběžné léčbě nefrotoxickými léky). Tato kontrola CrCL by měla být 1krát ročně při léčbě provedena i u osob starších 75 let a u pacientů s poruchou funkce ledvin [14]. Hepatální toxicitu, kterou projevoval jeho předchůdce přímý inhibitor trombinu ximelagatran (přípravek byl proto stažen výrobcem AstraZeneca z trhu), však dabigatran nemá.
Účinnost dabigatranu při prevenci TEN byla porovnávána s enoxaparinem v programu REVOLUTION. Dabigatran zde měl při primární prevenci TEN po totální náhradě kolenního nebo kyčelního kloubu srovnatelný účinek s LMWH enoxaparinem. Na základě těchto klinických studií je nyní dabigatran indikován v prevenci žilního tromboembolizmu po elektivní náhradě kolenního a kyčelního kloubu. Doporučená dávka je 220 mg jednou denně, resp. v určitých případech redukovaná dávka 150 mg jednou denně. Perorální léčbu je třeba zahájit během 1–4 hod po ukončení operace podáním jedné tobolky, poté je nutno pokračovat dvěma tobolkami jednou denně po celkovou dobu 10 dní (po elektivní náhradě kolenního kloubu) a 28–35 dní (po elektivní náhradě kyčelního kloubu), pokud nejsou krvácivé komplikace a je zabezpečena hemostáza [14]. S přípravkem proběhly i další studie. RE-COVER studie byla zaměřena na léčbu akutního žilního tromboembolizmu. Dabigatran v dávce 2krát 150 mg denně měl statisticky prokázanou noninferioritu proti warfarinu. Po šestiměsíční léčbě došlo u dabigatranové skupiny k 2,4% výskytu rekurence TEN, u warfarinu v 2,1 % (p < 0,001 pro noninferioritu). Při léčbě s warfarinem však bylo pozorováno více všech druhů krvácení. Další studie zaměřené na léčbu žilní TEN jsou RE-MEDY (po předchozí léčbě s warfarinem), studie 2. fáze RE-DEEM u pacientů s akutním koronárním syndromem ukázala sklon ke krvácení ve vztahu k výši dávky. Studie 3. fáze zatím zahájena nebyla [15].
Nynější nejrozšířenější indikací dabigatranu je však profylaxe tromboembolických mozkových příhod a systémové embolizace u nemocných s fibrilací síní. Vychází se zde z velmi dobrých výsledků studie RE-LY, která byla provedena u více než 18 000 pacientů s fibrilací síní. Byl zde porovnán efekt dvou dávek dabigatranu (110 mg nebo 150 mg 2krát denně) s warfarinem. Na základě dosažených výsledků byl pak dabigatran dne 1. 8. 2011 v Evropě schválen pro indikaci prevence cévní mozkové příhody a systémové embolie u dospělých pacientů s nevalvulární fibrilací síní s jedním nebo více následujícími rizikovými faktory: cévní mozková příhoda, tranzitorní ischemická ataka nebo systémová embolie v anamnéze, EF LK < 40 %, symptomatické srdeční selhání třídy II či vyšší dle klasifikace NYHA, věk ≥ 75 let, věk ≥ 65 let spojený s jedním z následujících onemocnění: diabetes mellitus, ischemická choroba srdeční nebo hypertenze. U pacientů s nižším rizikem krvácení (HAS-BLED skóre 0 až 2) je podle SPC [14] vhodná vyšší a účinnější dávka 150 mg 2krát denně, při vyšším riziku krvácení (HAS-BLED skóre ≥ 3) je bezpečnější nižší dávka 2krát 110 mg. U pacientů s jedním méně závažným rizikem TEN (dle CHADS2 skórovacího systému 1 bod) lze zvážit dabigatran v dávce 2krát 110 mg, která má stejnou účinnost jako antagonisté vitaminu K, ale nižší riziko krvácivých komplikací. V dávce 2krát 150 mg je dabigatran schválen k použití u nemocných s fibrilací síní i americkou FDA.
U dětí a mladistvých do 18 let se však dabigatran nedoporučuje z důvodu nedostatku údajů o bezpečnosti a účinnosti. U těhotných a v době kojení je kontraindikován také.
Dabigatran podobně jako předchozí nové přípravky nemá antidotum. Výrobce v případech klinicky závažného krvácení doporučuje léčbu přerušit a zjistit zdroj krvácení. Protože se dabigatran vylučuje převážně renálně, musí být udržována adekvátní diuréza. Dle úvahy ošetřujícího lékaře se zajistí vhodná podpůrná léčba, jako je chirurgická hemostáza a náhrada krevního objemu. Vzhledem k nízké vazbě na bílkoviny však lze dabigatran dialyzovat bez přidání antikoagulancia. Nyní byla uveřejněna zpráva o úspěšné hemodialýze při krvácení po provedeném bypassu spolu s náhradou insuficientní aortální chlopně u pacienta léčeného předtím dabigatranem v dávce 2krát 150 mg. Byl 3krát podáván i rekombinantní faktor VIIa, ale bez většího efektu na zástavu krvácení, podobně jako podání tranexamové kyseliny, 22 j. plazmy a četných převodů destiček a erytrocytové masy [16].
Ovlivnění koagulace dabigatranem lze v mimořádných situacích laboratorně monitorovat, během běžné léčby to opět není třeba. Přibližný údaj o intenzitě antikoagulačního účinku dabigatranu poskytuje aktivovaný parciální tromboplastinový čas (aPTT), který je snadno dostupný. Je zejména užitečný k detekci nadměrné antikoagulační aktivity dabigatranu. Výsledek testu aPTT > 80 s je v okamžiku minimální koncentrace dabigatranu (tj. v okamžiku, kdy má být podána jeho další dávka) spojen se zvýšeným rizikem krvácení. Nicméně aPTT test má omezenou citlivost a není vhodný pro přesné stanovení antikoagulačního účinku, zvláště při vysokých plazmatických koncentracích dabigatranu. V případě potřeby by měly být provedeny citlivější kvantitativní testy, jako je kalibrovaný dilutovaný trombinový čas Hemoclot® (Hyphen BioMed, Neuville-sur-Oise, Francie). Nález koncentrace dabigatranu v plazmě > 200 ng/ml (přibližně > 65 s) za 10–16 hod od podání předchozí dávky je spojen se zvýšeným rizikem krvácení [17]. Normální výsledek jiného orientačního koagulačního testu – trombinového času (TT) zase znamená, že není přítomen žádný klinicky významný antikoagulační účinek dabigatranu.
V tab. 1 jsou uvedeny v přehledu stručné údaje o „nových“ antikoagulanciích.
![Stručná charakteristika nových antikoagulancií [4,10,14].](https://www.kardiologickarevue.cz/media/cache/resolve/media_object_image_small/media/image/e5b4a49937f1695be9f18eb3fbc60f69.png)
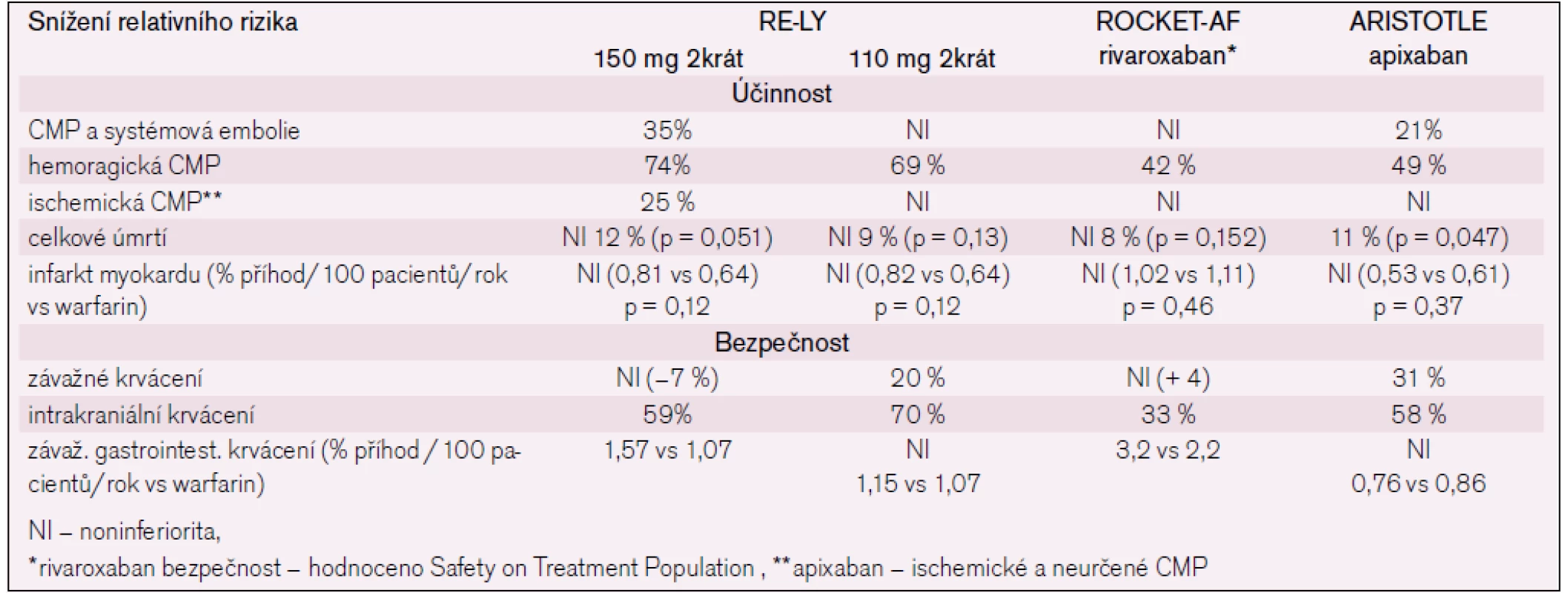
V tab. 2 jsou uvedeny výsledky použití „nových“ antikoagulancií při profylaxi kardioembolického iktu nebo systémové embolizace u nemocných s nevalvulární fibrilací síní.
Diskuze k použití „nových“ antikoagulancií
Jaké stanovisko je tedy dnes možné zaujmout k léčbě „novými“ antikoagulancii? Povolení léku k léčbě národními institucemi kontrolujícími léky, u nás je to SÚKL v návaznosti na EMA, ještě automaticky neznamená, že schválené léky budou při léčbě ve všech svých indikacích dle SPC doporučovány k léčbě i jednotlivými odbornými skupinami. U nás je to zejména Česká kardiologická společnost. Podle již citovaného Doporučení 9. konsenzu ACCP z února 2012 [1] jsou všechna tři nová antikoagulancia – dabigatran, rivaroxaban a apixaban doporučena k prevenci pooperační TEN po plánovaných ortopedických operacích – totální náhradě kyčelního nebo kolenního kloubu. Spolu s nimi je však v této indikaci stále možno použít i další antikoagulancia – nízkomolekulární hepariny (LMWH), fondaparinux, nefrakcionovaný heparin v nízkých dávkách, warfarin a kupodivu i aspirin (vše stupeň 1B). K léčbě žilní trombózy nebo plicní embolie zde zatím indikována nejsou. Při léčbě nemocných s nevalvulární fibrilací síní se středním a vysokým rizikem iktu (CHADS2 skóre ≥ 1, resp. ≥ 2) je pak při volbě antikoagulancia podle Doporučení 9. ACCP dávána již jednoznačně přednost dabigatranu (2krát 150 mg) před léčbou warfarinem (INR 2,0–3,0) (stupeň 2B) [18]. Americká Doporučení ACCF/AHA/HRS ve svém doplňku k léčbě fibrilace síní z roku 2011 [19] uvádějí dabigatran jako alternativu warfarinu (třída I, úroveň evidence B). Doporučení České kardiologické společnosti z roku 2011 [20] preferuje při léčbě fibrilace síní u nemocných warfarin, popřípadě připouští i „nová“ antitrombotika (dabigatran 2krát 150 nebo 2krát 110 mg/den). V předpokládané novelizaci pak připouští i jiná jako rivaroxaban nebo apixaban. Po zavedení stentu je však u nemocných s fibrilací síní jak v doporučeních 9. ACCP, tak i v Doporučení České kardiologické společnosti k trojkombinační léčbě spolu s aspirinem a clopidogrelem navrhován jen warfarin. Tato léčba je pak dále modifikována podle typu stentu nebo rizika krvácení HAS-BLED skóre.
Závěrem je nutno při hodnocení uplatnění „nových“ antikoagulancií v klinické praxi uvést, že s jejich používáním nejsou dlouhodobé zkušenosti. K léčbě byly povoleny teprve nedávno, před několika lety. To je málo, i takové terapeutické stálice, jakými jsou statiny, nám teď přinesly překvapení o možném riziku diabetu, a to i po 20 letech jejich používání v klinické praxi [21], a vyvolaly tak řadu nových studií, které teď potvrzují nebo vyvracejí toto podezření.
Pokud však v případě potřeby chybí rychlý a účinný způsob eliminace účinku „nových“ antikoagulancií, vede to u každého lékaře také k obavě z možného rizika nezvládnutelného krvácení v případě úrazu, urgentní operace apod. V případě polymorfního pacienta se pak monitorace efektu antikoagulace vhodnými laboratorními testy [15] nebo možnost úpravy dávky antikoagulancia jeví jako vhodnější způsob léčby než podávání jednotné dávky léku pro všechny, byť ve své účinnosti ověřené v klinických studiích na velkých souborech. Z tohoto hlediska je na tom tedy z „nových“ antikoagulancií zatím lépe dabigatran, kde podle výše rizika krvácení můžeme u léčeného pacienta volit mezi nižším nebo vyšším dávkováním. K uklidnění situace zde nyní přispěla i nová detailní studie nepotvrzující podezření na zvýšené riziko vzniku infarktu v porovnání s warfarinem [22].
Vypracováno za podpory RVO-VFN 64165/2012.
Doručeno do redakce 3. 4. 2012
Přijato po recenzi 16. 4. 2012
prof. MUDr. Jan Kvasnička, DrSc.
Trombotické centrum, ÚLBLD VFN v Praze
jan.kvasnicka@vfn.cz
Zdroje
1. Guyatt GH, Akl EA, Crowther M et al. American College of Chest Physicians Antithrombotic Therapy and Prevention of Thrombosis Panel. Executive Summary: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed. American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 2012; 141 (2 Suppl): 7S–47S.
2. Budnitz DS, Lovegrove MC, Shebab N et al. Emergency hospitalization for averse drug events in older Americans. N Engl J Med 2011; 365: 2002–2012.
3. Kvasnička J, Slíva J. Rivaroxaban. Farmakoterapie 2008; 4 : 381–385.
4. European Medicines Agency. SPC Xarelto. http://www.ema.europa.eu/docs/cs_CZ/document_library/EPAR_-_Product_Informat ion/human/000944/WC500057108.pdf.
5. Eerenberg ES, Kamphuisen PW, Sijpkens MK et al. Reversal of rivaroxaban and dabigatran by prothrombin complex concentrate: a randomized, placebo-controlled, crossover study in healthy subjects. Circulation 2011; 124: 1573–1579.
6. Godier A, Miclot A, Le Bonniec B et al. Evaluation of prothrombin complex concentrate and recombinant activated factor VII to reverse rivaroxaban in a rabbit model. Anesthesiology 2012; 116: 94–102.
7. Patel MR, Mahaffey KW, Garg J et al. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med 2011; 365: 883–891.
8. EINSTEIN Investigators, Bauersachs R, Berkowitz SD, Brenner B et al. Oral rivaroxaban for symptomatic venous thromboembolism. N Engl J Med 2010; 363: 2499–2510.
8. The EINSTEIN–PE Investigators. Oral Rivaroxaban for the Treatment of Symptomatic Pulmonary Embolism. N Engl J Med 2012 [Epub ahead of print].
9. Mega JL, Braunwald E, Wiviott SD et al. ATLAS ACS 2–TIMI 51 Investigators. Rivaroxaban in patients with a recent acute coronary syndrome. N Engl J Med 2012; 366: 9–19.
10. European Medicines Agency. SPC Eliquis. http://www.ema.europa.eu/docs/cs_CZ/document_library/EPAR_-_Product_Informat ion/human/002148/WC500107728.pdf.
11. Bassand JP. Review of atrial fibrillation outcome trials of oral anticoagulant and antiplatelet agents. Europace 2012; 14: 312–324.
12. Alexander JH, Lopes RD, James S et al. APPRAISE-2 Investigators. Apixaban with antiplatelet therapy after acute coronary syndrome. N Engl J Med 2011; 365: 699–708.
13. Kvasnička J, Slíva J. Dabigatran. Farmakoterapie 2008; 4: 359–365.
14. European Medicines Agency. SPC Pradaxa. http://www.ema.europa.eu/docs/cs_CZ/document_library/EPAR_-_Product_Informat ion/human/000829/WC500041059.pdf.
15. Steffel J, Braunwald E. Novel oral anticoagulants: focus on stroke prevention and treatment of venous thrombo-embolism. Eur Heart J 2011; 32: 1968–1976.
16. Warketin TE, Margetts P, Connolly SJ et al. Recombinant factor VIIa (rFVIIa) and hemodialysis to manage massive dabigatran-associated postcardiac sugery bleeding. Blood 2012; 119: 2172–2173.
17. Avecilla ST, Ferrell C, Chandler WL et al. Plasma-diluted thrombin time to measure dabigatran concentrations during dabigatran etexilate therapy. Am J Clin Pathol 2012; 137: 572–574.
18. You JJ, Singer DE, Howard PA et al. American College of Chest Physicians. Antithrombotic Therapy for Atrial Fibrillation: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed. American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 2012; 141 (2 Suppl): e531S–e575S.
19. Page RL, Slotwiner DJ, Stevenson WG et al. 2011 ACCF/AHA/HRS Focused Update on the Management of Patients With Atrial Fibrillation (Update on Dabigatran). A Report of the American College of Cardiology Foundation Foundation/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol 2011; 57; 1330–1337.
20. Čihák R, Heinc P, Haman L et al. Fibrilace síní. Doporučený diagnostický a léčebný postup České kardiologické společnosti vypracovaný Pracovní skupinou arytmie a trvalé kardiostimulace. Cor Vasa 2011; 53 (Suppl 1): 27–52.
21. Culver AL, Ockene IS, Balasubramanian R et al. Statin use and risk of diabetes mellitus in postmenopausal women in the Women’s Health Initiative. Arch Intern Med 2012; 172: 144–152.
22. Hohnloser SH, Oldgren J, Yang S et al. Myocardial Ischemic Events in Patients With Atrial Fibrillation Treated With Dabigatran or Warfarin in the RE-LY (Randomized Evaluation of Long-Term Anticoagulation Therapy) Trial. Circulation 2012; 125: 669–676.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2012 Číslo 2
Nejčtenější v tomto čísle
- Antiagregační a antikoagulační léčba – základní principy
- Antikoagulační terapie a fibrilace síní
- Kam se ubírá současný vývoj léků ovlivňujících krevní srážení?
- Současné doporučení k antiagregační léčbě v neurologii
