Patofyziologie a diagnóza obstrukce u hypertrofické kardiomyopatie
Pathophysiology and diagnosis of obstruction in hypertrophic cardiomyopathy
Intraventricular obstruction is one of the fundamental pathophysiological manifestations of hypertrophic cardiomyopathy with significant clinical impact. Therefore, it is important to actively search for it during examination, even with the use of various provoking tests. In this article we would like to summarize current knowledge about its pathophysiology and diagnostic possibilities, including the use of provocative tests.
Keywords:
hypertrophic cardiomyopathy – obstruction – diagnosis – echocardiography
Autoři:
D. Zemánek
Působiště autorů:
Kardiologická klinika 2. LF UK a FN v Motole, Praha
Vyšlo v časopise:
Kardiol Rev Int Med 2015, 17(1): 7-10
Kategorie:
Kardiologická revue
Souhrn
Nitrokomorová obstrukce patří k základním patofyziologickým projevům hypertrofické kardiomyopatie s významným klinickým dopadem. Proto je důležité při vyšetření po ní aktivně pátrat, třeba i za pomoci použití různých provokačních testů. V tomto článku bychom chtěli shrnout současné poznatky o její patofyziologii a také o možnostech diagnostiky včetně použití provokačních testů.
Klíčová slova:
hypertrofická kardiomyopatie – obstrukce – diagnóza – echokardiografie
Nitrokomorová obstrukce patří k základním patofyziologickým projevům hypertrofické kardiomyopatie (HCM). Její význam spočívá v tom, že se podílí na klinické symptomatologii pacientů s HCM a také představuje rizikový faktor z hlediska jejich prognózy. Její úspěšná eliminace pak vede ke zlepšení symptomů a podle některých údajů také prognózy u těchto pacientů. Výskyt je udáván v literatuře v širokém rozmezí od 20 do 70 % [1]. Tomu odpovídají také naše vlastní data, kdy byla obstrukce přítomna u 71 % pacientů vyšetřených ve FN Motol pro HCM [2]. Její prevalence závisí na výběru vyšetřovaného souboru a použití provokačních testů. V tomto článku bychom chtěli shrnout současné poznatky o její patofyziologii a také možnostech diagnostiky.
Patofyziologie
Samotná obstrukce může být lokalizována jednak ve výtokovém traktu levé komory (LVOT) a/ nebo ve středních etážích levé komory (LK) – midventrikulárně. Velmi vzácně se také vyskytuje ve výtokovém traktu pravé komory. V LK je obstrukce v LVOT přibližně 10× častější. Problematika midventrikulární obstrukce bude probrána v samostatné části článku a následující text se bude věnovat obstrukci v LVOT.
Historicky se u ní předpokládal sfinkterový mechanizmus vzniku. Později na základě hemodynamických katetrizačních údajů a echokardiografie byla vytvořena dnes již částečně překonaná teorie na podkladě Venturiho efektu. Podle této teorie se na obstrukci podílí lokální podtlak v LVOT, který vede k nasávání předního cípu mitrální chlopně a jejího závěsného aparátu. Tato teorie vycházela z pozorovaného vztahu mezi přítomností systolického dopředného pohybu mitrální chlopně (SAM), který spočívá v přiblížení nebo kontaktu předního cípu mitrální chlopně a bazální části septa LK během systoly, a přítomností obstrukce [3].
Dnes se předpokládá, že je tento mechanizmus mnohem komplexnější a Venturiho efekt hraje jen podpůrnou úlohu [4]. Předpokladem vzniku obstrukce u HCM je hypertrofie stěn, především mezikomorového septa, která je často spojena se změnou tvaru dutiny LK. Kromě toho jsou oba papilární svaly posunuty obvykle více dopředu, a tak je celý subvalvulární mitrální závěsný aparát posunut směrem k LVOT a septu. Navíc je současně přední cíp mitrální chlopně u pacientů s HCM prodloužený ve srovnání s běžnou populací, což vede k určité nadbytečnosti závěsného aparátu. Tyto podmínky vedou k tomu, že při systole LK dochází k odklonění krevního toku z optimálního směru pro hypertrofii septa a abnormální hypertrofické papilární svaly. Tomuto odkloněnému toku se do cesty staví závěsný aparát předního cípu a samotný zvětšený přední cíp. Tyto struktury jsou pak následně krevním proudem tlačeny směrem k septu, přičemž celý LVOT se zároveň zužuje. Akcelerace průtoku při vznikajícím zužování ústí pak tuto situaci dále zhoršuje. Tento mechanizmus zjednodušeně připomíná „zavírání dveří v průvanu“. Svůj vliv na to může mít také úhel, který svírá osa LK a aorty, kdy pacienti s obstrukcí mají tento úhel menší než bez obstrukce [5]. Ten by také mohl být příčinou vzniku obstrukce u starších pacientů s tzv. septum sigmoideum, kteří jinak mají hypertrofii LK jen mírnou a záchyt sarkomerických mutací (jako příčiny HCM) je u nich nízký.
Mechanizmus vzniku obstrukce je tedy poměrně komplexní, a tak nepřekvapí, že je tento jev velmi variabilní a je ovlivněn aktuálním hemodynamickým stavem. Mezi faktory zvyšující obstrukci patří snížení předtížení (dehydratace, hypovolemie, Valsalvův manévr), snížení dotížení (vazodilatační látky) a zvýšení kontraktility (pozitivně ionotropní látky). Naproti tomu zvýšení předtížení (volumexpanze), dotížení (vazokonstrikční látky) a snížení kontraktility (negativně ionotropní látky) vedou k poklesu velikosti gradientu u obstrukce. Variabilita měření gradientu v po sobě následujících dnech přesahuje rozptyl hodnot kolem 50 % [6]. Ke zvýšení senzitivity jednorázového vyšetření si proto pomáháme tzv. provokačními manévry. Jejich principem je změna hemodynamických podmínek během vyšetření na podkladě změn předtížení, dotížení nebo kontraktility, které vedou ke vzniku obstrukce.
Diagnóza
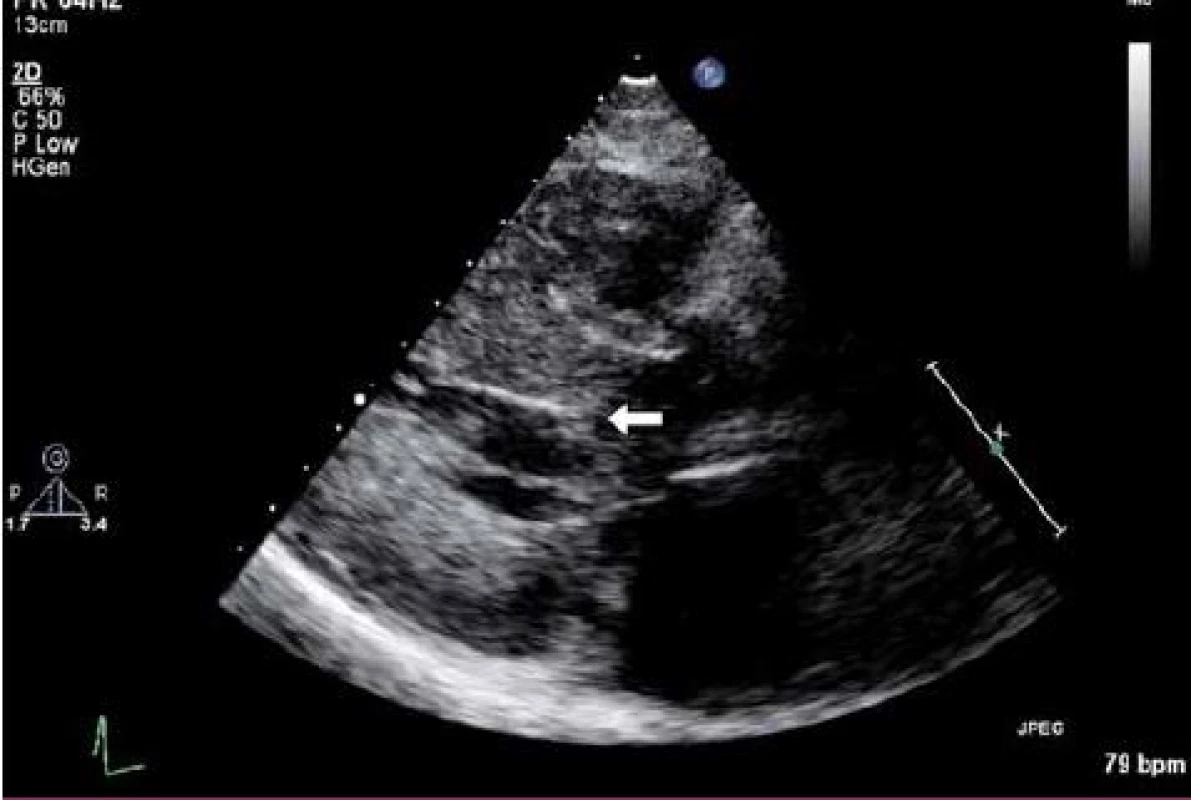
Základní vyšetřovací metodou nitrokomorové obstrukce u HCM zůstává i v dnešní době echokardiografie. Kromě samotné morfologie srdce totiž dokáže zobrazit turbulentní proudění odpovídající přítomné obstrukci a především ji můžeme kvantifikovat. Ze změřené rychlosti můžeme pomocí Bernoulliho rovnice získat tlakový gradient v místě obstrukce. Při vlastním vyšetření se zaměřujeme na hodnocení morfologie septa (tvar, rozsah hypertrofie), mitrální chlopně, pozici papilárních svalů a přítomnost SAM. Hodnocení hypertrofie septa, velikosti mitrální chlopně a především SAM běžně hodnotíme v parasternální projekci na dlouhou srdeční osu (obr. 1). Naopak velikost tlakového gradientu a tvar septa hodnotíme obvykle v pětidutinové hrotové projekci, ale SAM je zde také patrný. Morfologické hodnocení LK je velmi důležité především proto, že nám umožňuje zvolit optimální strategii při léčbě obstrukce. V případě těžké komplexní hypertrofie se budeme klonit spíše k chirurgické myektomii, naopak u izolované hypertrofie bazálního septa (septum sigmoideum) bude metodou volby katetrizační alkoholová septální ablace. Současně bychom se měli zaměřit na mitrální regurgitaci, která je často spojena s přítomností obstrukce v LVOT. Pokud se přední cíp vytahuje během systoly do LVOT, tak v případě, že kratší zadní cíp není schopen kompenzovat tento posun, dochází k posunu zóny koaptace, a tak ke vzniku mitrální regurgitace [7]. Regurgitační proud proto u HCM směruje typicky posterolaterálně a dosahuje maxima v pozdní fázi systoly. Tento fakt má důležitý klinický význam, neboť v případě centrální regurgitace je třeba vždy myslet na jiný mechanizmus jejího vzniku a nelze automaticky předpokládat, že dojde k její úpravě po izolované úspěšné eliminaci obstrukce v LVOT, a proto by měli být tito pacienti také přednostně indikováni k chirurgické myektomii.
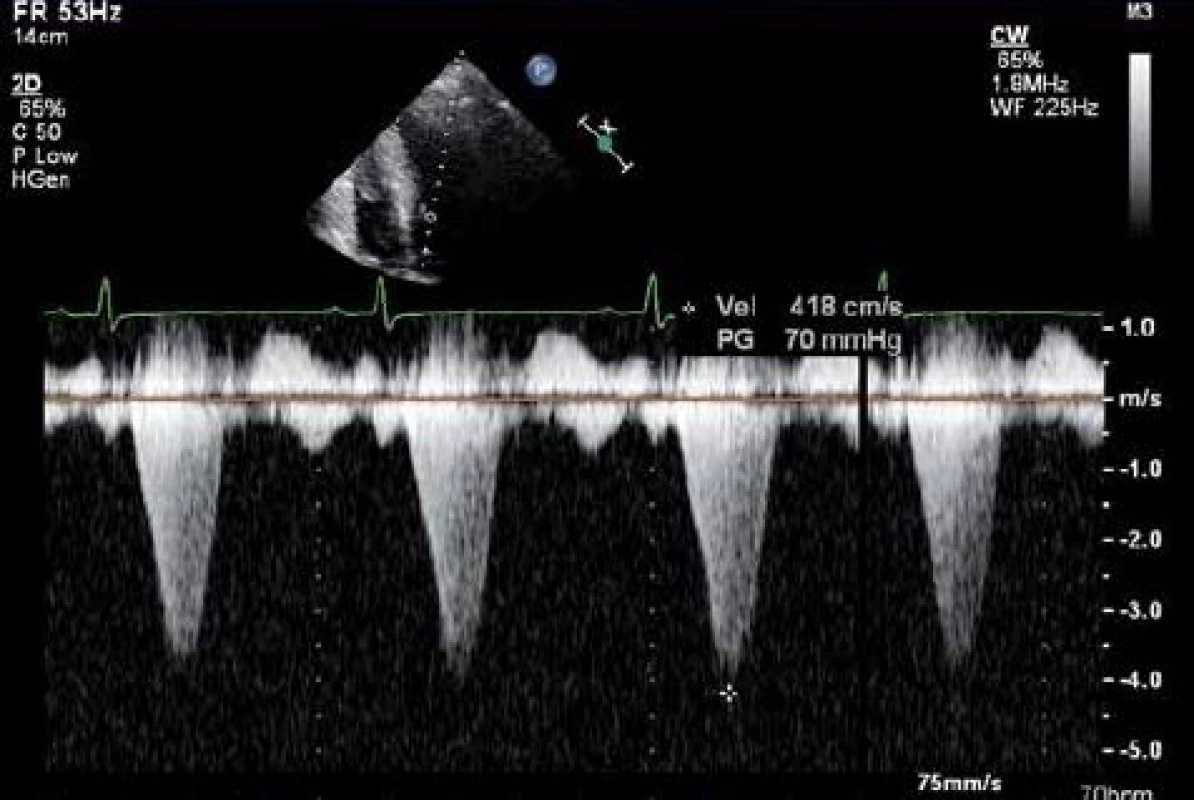
Vlastní hodnocení potom provádíme pomocí pulzního a kontinuálního dopplerovského vyšetření, které nám umožňuje kvantifikovat velikost nitrokomorové obstrukce a lokalizovat místo jejího vzniku. Pulzní vyšetření umožňuje přesněji určit místo obstrukce (nehrozí možnost záměny gradientu na aortální chlopni s obstrukcí v LVOT nebo s gradientem na mitrální chlopni při regurgitaci), na druhé straně je jeho použití omezeno Nyquistovým limitem při vyšetření vysokých rychlostí. V praxi potom používáme kombinaci obou technik, kdy pomocí pulzního vyšetření lokalizujeme místo obstrukce a pomocí kontinuálního záznamu kvantifikujeme velikost obstrukce. Dopplerovská křivka u obstrukce má v typickém případě pozdně systolický vrchol na rozdíl např. od aortální stenózy, kde je symetrická (obr. 2).
Na základě změřených hodnot maximálního gradientu v LVOT pak rozdělujeme pacienty částečně z didaktických důvodů do tří skupin: 1) s klidovou obstrukcí (gradient větší než 30 mm Hg v klidu), 2) s latentní obstrukcí (bez klidové obstrukce, ale s gradientem větším než 30 mm Hg po provokaci) a 3) bez obstrukce [1].
Provokační testy
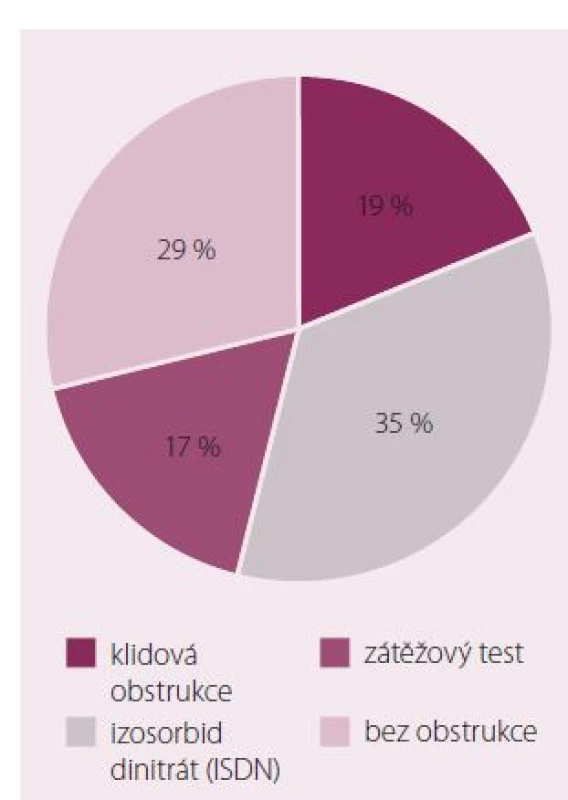
Jak již bylo uvedeno v kapitole o patofyziologii, je obstrukce v LVOT dynamický proces s řadou ovlivňujících faktorů, a tak může být variabilita měřených výsledků velmi vysoká [6]. U stejného pacienta můžeme při jednom vyšetření zjistit významnou obstrukci a při dalším vyšetření může být tentýž pacient bez obstrukce. Někteří autoři proto doporučují vyšetření několikrát opakovat. V klinické praxi je užitečné použití provokačních testů, které významně zvyšují senzitivitu jednorázového vyšetření. V práci Marona et al byla prevalence významné klidové obstrukce 37 % a dalších 33 % pacientů mělo obstrukci po provokačních testech [1]. V našem souboru konsekutivních pacientů byla obstrukce v LVOT přítomna při klidovém vyšetření u 21 % pacientů, po provokaci sublinguální aplikací izosorbid dinitrátu vzestoupila její prevalence na 55 % a při použití zátěžového testu běhátkem až na 71 % (obr. 3) [2]. Tato data jednoznačně potvrzují, že klidové vyšetření by mělo být doplněno některým z provokačních testů.
Mezi nejčastěji používané provokační testy patří měření po extrasystole, během Valsalvova manévru, po sublinguální aplikaci nitrátu nebo inhalaci amylnitritu, při infuzi katecholaminů a na vrcholu nebo těsně po ukončení fyzické zátěže. Měření po extrasystole se hodí především do katetrizačních laboratoří, neboť pomocí katetru v LK lze jednoduše způsobit komorovou extrasystolu a naopak při echokardiografickém vyšetření se jedná spíše o náhodu.
Valsalvův manévr je jednoduchý, časově nezatěžující test. Problémem může být, že během něj dochází k posunu srdce a plic v hrudníku, a tak nemusí být pacient vždy dobře vyšetřitelný. Kromě toho také manévr vyžaduje určitou spolupráci pacienta, kterou nejsme schopni kontrolovat. Navíc není plná korelace se zátěžovou echokardiografií [8].
Provokace obstrukce pomocí infuze katecholaminů, jako například dobutaminu nebo izoprenalinu, vede pomocí zvýšené kontraktility myokardu také ke vzniku obstrukce v LVOT [9]. Nicméně v dnešní době se pro určité nebezpečí vzniku arytmií rutinně nepoužívá a navíc není přesně jasná korelace vzniku obstrukce k symptomům a klinickému stavu pacientů. Určitou výjimku může představovat použití přímo v katetrizační laboratoři, kde jsou jinak možnosti provokačních testů omezené [10].
Další alternativou je použití léků snižujících preload a afterload, např. pomocí vazodilatace. Inhalace amylnitritu v jedné studii vedla nejen ke zvýšení výskytu obstrukce u HCM, ale navíc tento vzestup částečně koreloval s výskytem obstrukce při použití zátěžového testu [11]. Tato metoda je používána ve Spojených státech amerických, nicméně v České republice není amylnitrit registrován a navíc má nežádoucí psychoaktivní účinky. Proto se v České republice používá sublinguální aplikace nitrátu (izosorbid dinitrát). V našem souboru nemocných vedla jeho aplikace k významnému vzestupu gradientu ve srovnání s klidovým vyšetřením a jeho pozitivita plně korelovala se zátěžovou echokardiografií [2]. Tato práce také prokázala, že aby bylo vyšetření validní, je třeba měření posunout o 5 až 10 min od aplikace léku, aby se efekt nitrátu mohl plně projevit. Nevýhodou aplikace nitrátu ve srovnání se zátěžovou echokardiografií byla nižší senzitivita. V práci zaměřené na jeho srovnání s Valsalvovým manévrem vedla aplikace izosorbid dinitrátu k častějšímu a většímu vzestupu maximálního gradientu v LVOT, nicméně jako nejúčinnější se ukázala kombinace těchto testů, neboť jejich efekt se potencuje [12].
Zátěžový test (běhátko, ergometr) je metodou nejsenzitivnější a navíc se nejvíc přibližuje fyziologickým podmínkám vzniku obstrukce a symptomů v běžném životě pacientů. Vzhledem k jeho relativní časové a logistické náročnosti jej rezervujeme pro pacienty, u nichž nedošlo ke vzniku obstrukce při ostatních provokačních testech nebo u nichž existují určité diagnostické rozpaky s jejich interpretací vztažené ke klinickému obrazu. Otázkou, která se nově diskutuje, je vlastní provedení zátěžového testu a přítomnost tzv. paradoxní odpovědi na zátěž. V roce 2013 byl publikován článek francouzských autorů, kteří prováděli vyšetření pomocí bicyklové ergometrie u pacientů vleže se současným průběžným záznamem gradientu v LVOT. Autoři vyšetřili 107 pacientů s HCM bez klidové obstrukce, z nichž u 38 pacientů vznikla během zátěže obstrukce (vrcholový gradient ≥ 30 mm Hg). Z těchto 38 pacientů došlo následně u devíti pacientů k následnému poklesu obstrukce během zátěže. Tato skupina pacientů byla v běžném životě méně symptomatická, měla větší objem LK a během zátěže u nich došlo k většímu vzestupu systémového krevního tlaku [13]. Autoři tento nově pozorovaný jev vysvětlují špatnou metodikou předchozích studií, kdy obstrukce byla měřena pouze na vrcholu zátěže nebo těsně po ní, a tak tento jev nebyl pozorován. Tato práce však byla podrobena kritice, protože pozice vleže při zátěži není fyziologická. Dochází při ní totiž k odlišnému plnění LK než ve vzpřímené pozici. Pozorovaný jev by tak mohl být důsledkem tohoto faktu [14]. Proto tato otázka zůstává nadále otevřená a bude potřeba, aby další studie tuto teorii potvrdily, nebo vyvrátily.
Na našem pracovišti používáme při vyšetřování pacientů s HCM tento postup. U pacientů, u kterých v klidu není přítomna významná obstrukce, provedeme během echokardiografického vyšetření Valsalvův manévr. Pokud stále není přítomna významná obstrukce, aplikujeme sublinguálně izosorbid dinitrát. Po uplynutí přibližně 10 min provádíme nové měření, které dle potřeby doplňujeme provedením nového Valsalvova manévru. Pokud je pacient symptomatický a pomocí těchto provokačních testů byla prokázána obstrukce, tak ho již dále nevyšetřujeme. V případě, že je symptomatický a obstrukce nebyla dosud vyvolána nebo pokud přetrvávají nejasnosti například o vztahu symptomů a obstrukce, provádíme zátěžovou echokardiografii (obr. 4).
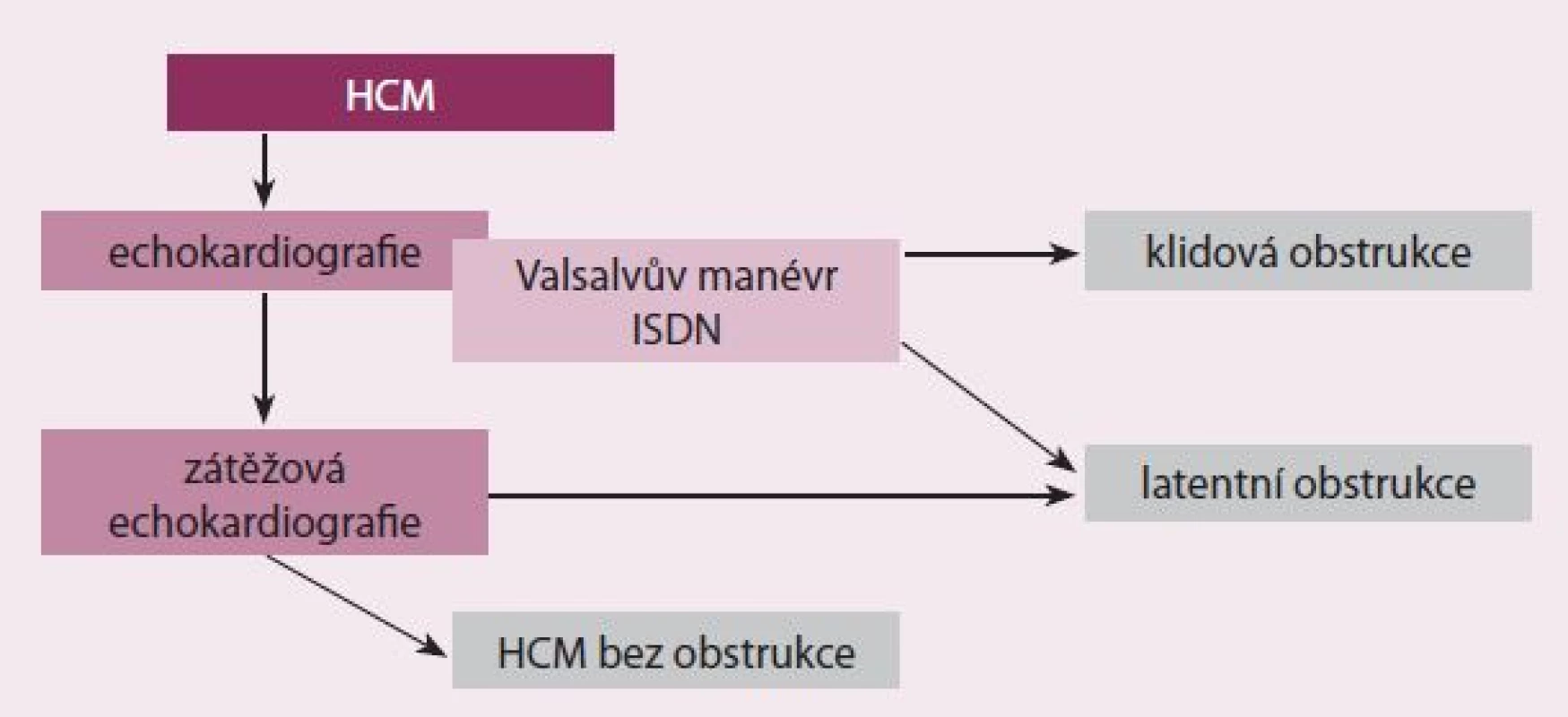
Midventrikulární obstrukce
Kromě obstrukce v LVOT popsané výše můžeme nalézt u HCM také obstrukci ve střední části LK. Tato obstrukce je asi 10× méně častá a přibližně v polovině případů je kombinována s obstrukcí v LVOT. Mechanizmus jejího vzniku připomíná původní sfinkterovou teorii, na které se také podílí posun hypertrofických papilárních svalů, které během systoly komor prakticky obliterují dutinu LK. Vyskytuje se tedy především u pacientů s komplexní masivní hypertrofií LK. Vznikající gradient nebývá obvykle tak vysoký jako u obstrukce v LVOT. Přesto je její přítomnost spojena se zhoršenou prognózou z hlediska vývoje terminálního srdečního selhání a také náhlé srdeční smrti [15]. Přítomnost midventrikulární obstrukce je také často spojena s nálezem apikálního aneuryzmatu LK, který představuje sám o sobě rizikový faktor výskytu náhlé srdeční smrti [16]. Obecně platí, že u pacientů s midventrikulární obstrukcí není alkoholová septální ablace indikována, ale také výsledky chirurgické myektomie jsou horší.
Závěr
Vyšetřování obstrukce je důležitou součástí posuzování pacienta s HCM. V případě, že se jedná o symptomatického pacienta a není přítomna klidová obstrukce, je nutné použít různé provokační testy, abychom mohli správně nasměrovat další léčbu.
Podpořeno MZ ČR – RVO, FN v Motole 00064203 a z Evropského sociálního fondu a státního rozpočtu České republiky – Projekt ICRC Human Bridge – podpora kvalitních týmů výzkumu a vývoje pomocí vzniku postdoktorských pozic (CZ.1.07/2.3.00/30.0023).
Doručeno do redakce: 11. 1. 2015
Přijato po recenzi: 29. 1. 2015
doc. MUDr. David Zemánek, Ph.D.
www.fnmotol.cz
david.zemanek@seznam.cz
Zdroje
1. Maron MS, Olivotto I, Zenovich AG et al. Hypertrophic cardiomyopathy is predominantly a disease of left ventricular outflow tract obstruction. Circulation 2006; 114: 2232– 2239.
2. Zemánek D, Tomašov P, Homolová S et al. Sublingual isosorbide dinitrate for the detection of obstruction in hypertrophic cardiomyopathy. Eur J Echocardiogr 2011; 12: 684– 687. doi: 10.1093/ ejechocard/ jer115.
3. Maron BJ, Maron MS, Wigle ED et al. The 50‑year history, controversy, and clinical implications of left ventricular outflow tract obstruction in hypertrophic cardiomyopathy from idiopathic hypertrophic subaortic stenosis to hypertrophic cardiomyopathy: from idiopathic hypertrophic subaortic stenosis to hypertrophic cardiomyopathy. J Am Coll Cardiol 2009; 54: 191– 200. doi: 10.1016/ j.jacc.2008.11.069.
4. Sherrid MV, Chaudhry FA, Swistel DG. Obstructive hypertrophic cardiomyopathy: echocardiography, pathophysiology, and the continuing evolution of surgery for obstruction. Ann Thorac Surg 2003; 75: 620– 632.
5. Martin R, Lairez O, Boudou N et al. Relation between left ventricular outflow tract obstruction and left ventricular shape in patients with hypertrophic cardiomyopathy: a cardiac magnetic resonance imaging study. Arch Cardiovasc Dis 2013; 106: 440– 447. doi: 10.1016/ j.acvd.2013.05.002.
6. Kizilbash AM, Heinle SK, Grayburn PA. Spontaneous variability of left ventricular outflow tract gradient in hypertrophic obstructive cardiomyopathy. Circulation 1998; 97: 461– 466.
7. Yu EH, Omran AS, Wigle ED et al. Mitral regurgitation in hypertrophic obstructive cardiomyopathy: relationship to obstruction and relief with myectomy. J Am Coll Cardiol 2000; 36: 19– 25.
8. Jensen MK, Havndrup O, Pecini R et al. Comparison of Valsalva manoeuvre and exercise in echocardiographic evaluation of left ventricular outflow tract obstruction in hypertrophic cardiomyopathy. Eur J Echocardiogr 2010; 11: 763– 769. doi: 10.1093/ ejechocard/ jeq063.
9. Braunwald F, Oldham HN, Ross J et al. Hemodynamic alterations in idiopathic hypertrophic subaortic stenosis induced by sympathomimetic drugs. Am J Cardiol 1962; 10: 489– 495.
10. Elesber A, Nishimura RA, Rihal CS et al. Utility of isoproterenol to provoke outflow tract gradients in patients with hypertrophic cardiomyopathy. Am J Cardiol 2008; 101: 516– 520. doi: 10.1016/ j.amjcard.2007.09.111.
11. Marwick TH, Nakatani S, Haluska B et al. Provocation of latent left ventricular outflow tract gradients with amyl nitrite and exercise in hypertrophic cardiomyopathy. Am J Cardiol 1995; 75: 805– 809.
12. Zemánek D, Tomašov P, Bělehrad M et al. Comparison of sublingual isosorbide dinitrate and Valsalva maneuver for the detection of obstruction in hypertrophic cardiomyopathy. Arch Med Sci 2015; [in press] doi: 10.5114/ aoms.2015.47096.
13. Lafitte S, Reant P, Touche C et al. Paradoxical response to exercise in asymptomatic hypertrophic cardiomyopathy: a new description of outflow tract obstruction dynamics. J Am Coll Cardiol 2013; 62: 842– 850. doi: 10.1016/ j.jacc.2013.06.007.
14. Dimitrow PP, Cotrim C, Cheng TO. The importance of upright posture in exercise testing and training for patients with hypertrophic cardiomyopathy. Eur J Prev Cardiol 2014; 108: 614.
15. Minami Y, Kajimoto K, Terajima Y et al. Clinical implications of midventricular obstruction in patients with hypertrophic cardiomyopathy. J Am Coll Cardiol 2011; 57: 2346– 2355. doi: 10.1016/ j.jacc.2011.02.033.
16. Maron MS, Finley JJ, Bos JM et al. Prevalence, clinical significance, and natural history of left ventricular apical aneurysms in hypertrophic cardiomyopathy. Circulation 2008; 118: 1541– 1549. doi: 10.1161/ CIRCULATIONAHA.108.781401.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2015 Číslo 1
Nejčtenější v tomto čísle
- TDM digoxinu v klinické praxi
- Lékové interakce a současná klinická praxe
- Srdeční resynchronizační terapie – kdy a u koho ji v současnosti indikovat?
- TDM antibiotik v klinické praxi
