PCSK9 inhibitory v klinické praxi – update
PCSK9 inhibitors in clinical practice – update
PCSK9 inhibitors belong to the new and extremely efficient lipid-lowering agents, which significantly not only decrease low-density lipoprotein (LDL) cholesterol and other aterogenic lipids including lipoprotein (a), but also significantly lower cardiovascular mortality and morbidity. These drugs are human monoclonal antibodies which block the activity of proprotein convertase subtilisin/kexin type 9 (PCSK9 inhibitors). Even though the PCSK9 inhibitors were approved for clinical use in the Czech Republic in autumn 2015, their prescription was only enabled on 1 June 2018. Recently, the first data from the therapy by PCSK9 inhibitors in real clinical praxis has been collected and evaluated. The following case reports of patients with hypercholesterolemia from our out-patient clinic for the lipid disorders document our recent experience with the PCSK9 inhibitor therapy.
Keywords:
Cholesterol – metabolism of LDL cholesterol – subtilisin/ kexin type 9 proprotein convertase
Autoři:
Blaha V.; Víšek J.
Působiště autorů:
III. interní gerontometabolická klinika LF UK a FN Hradec Králové
Vyšlo v časopise:
Kardiol Rev Int Med 2019, 21(3): 163-167
Souhrn
Inhibitory PCSK9 patří mezi nová a mimořádně účinná hypolipidemika, která signifikantně snižují nejen nízko-denzitní lipoprotein (LDL) cholesterol a další aterogenní lipidy vč. lipoproteinu (a), ale také významně snižují kardiovaskulární mortalitu a morbiditu. Jedná se o humánní monoklonální protilátky, blokující účinek proproteinových konvertáz subtilisin/ kexinového typu (inhibitory PCSK9). Ačkoliv byly tyto léčivé přípravky schváleny ke klinickému využití v ČR již na podzim roku 2015, možnost preskribce byla umožněna teprve od 1. 6. 2018. V současné době tedy sbíráme a hodnotíme první zkušenosti s využitím inhibitorů PCSK9 v reálné klinické praxi. Předkládané kazuistiky pacientů s hypercholesterolemií z naší ambulance pro poruchy metabolizmu lipidů dokumentují naše dosavadní zkušenosti s léčbou inhibitory PCSK9.
Klíčová slova:
Cholesterol – metabolizmus LDL cholesterolu – proprotein konvertáza subtilisin/ kexin typ 9
Úvod
Zvýšená plazmatická koncentrace nízko-denzitního lipoprotein cholesterolu (LDL-c) je kauzálním faktorem aterosklerotických kardiovaskulárních onemocnění (KVO) a podmiňuje vznik a rozvoj KV příhod, vč. infarktů myokardu (IM) a cévních mozkových příhod (CMP), které jsou spojené s významnou morbitidu a mortalitou postižených pacientů [1]. U některých pacientů s hypercholesterolemií lze dosáhnout snížení LDL-c pomocí dietních opatření a úpravou životního stylu, ale řada pacientů vyžaduje k dosažení klinicky relevantních hodnot LDL-c farmakoterapii hypolipidemiky. Léčba statiny tvoří standardní základ farmakoterapie a její účinnost byla prověřena v řadě klinických studií. Někteří léčení pacienti však nedosáhnou adekvátního snížení LDL-c. Ve velké globální kohortě dosáhlo při léčbě statiny cílových hodnot LDL-c dle individuálního rizika jen 27 % pacientů, a ve skupině nemocných s velmi vysokým KV rizikem dokonce jen 22 % osob [2]. Zúčastněné odborné autority (European Society of Cardiology/ European Atherosclerosis Society) doporučují léčbu individualizovat dle pacientova KV rizika [3,4]. U pacientů, kde nelze dosáhnout snížení LDL-c při léčbě statiny v první linii, lze do kombinace předepsat ezetimib nebo monoklonální protilátky proti PCSK9 (proproteinové konvertázy subtilisin/ kexin typ 9), tj. inhibitory PCSK9. Dva z inhibitorů PCSK9, evolocumab (v dávkování 140 mg 1× za 2 týdny nebo 420 mg 1× za měsíc s.c.) a alirocumab (v dávkování 75 mg/ 150 mg 1× za 2 týdny nebo 300 mg 1× za měsíc s.c.) jsou od roku 2015 schváleny pro klinické využití jak v EU, tak v USA jako komplementární terapie k maximální tolerované dávce statinu u pacientů adherujících k dietním a režimovým opatřením, kteří vyžadují aditivní snížení LDL-c. Oba inhibitory PCSK9 prokázaly svoji účinnost v klinických studiích, kde léčba evolocumabem spolu se statiny vedla ke snížení LDL-c o dalších až 75 % ve srovnání s léčbou statiny samotnými, a léčba alirocumabem spolu se statiny vedla ke snížení LDL-c o dalších až 58 % ve srovnání s léčbou statiny samotnými [5,6].
Snížení LDL-c má dlouhodobý charakter, a co je důležité, není provázeno neadekvátním výskytem nežádoucích účinků při déledobé expozici [7]. Ve sledování japonských autorů, kteří kontrolovaně podávali evolocumab po dobu 5 let, bylo po celou dobu sledování dosaženo snížení LDL-c o 58– 62,7 % (obr. 1) [8], bezpečnostní profil se nelišil od situace před podáváním evolocumabu. Protilátky proti evolocumabu byly přechodně detekovány u 3 pacientů z 556, u žádného pacienta nebyly zjištěny neutralizující protilátky.
![Vliv dlouhodobé léčby evolocumabem na snížení LDL-c. Upraveno podle [8].](https://www.kardiologickarevue.cz/media/cache/resolve/media_object_image_small/media/image_pdf/5fc02cfd110aded9bc68b227743d50ad.png)
Randomizované kontrolované studie s oběma PCSK9 inhibitory v kombinaci se statiny prokázaly snížení rizika KV příhod jak u pacientů s aterosklerotickým KVO, tak po akutním koronárním syndromu [9]. Kromě toho jsou k dispozici také data o snížení celkové mortality v případě alirocumabu [10], ačkoliv takové údaje nebyly pozorovány v případě evolocumabu vs. placebo [9]. Výsledky studie FOURIER (Further Cardiovascular Outcomes Research with PCSK9 Inhibition in Subjects with Elevated Risk) pak prokázaly u pacientů s aterosklerotickým KVO podobnou redukci výskytu KV příhod, ať už měli vstupní koncentraci LDL-c < 1,80 nebo ≥ 1,80 mmol/ l nebo zda byli pacienti na maximální vs. submaximální dávce léčby statiny [11].
V současné době máme také dispozici již řadu pozorování a kazuistik z reálné klinické praxe. Američtí autoři hodnotili data získaná z 18 zdravotnických systémů (Patient-centered Clinical Research Network (PCORnet) [12]. V souboru bylo hodnoceno > 17,5 milionu dospělých, a 3,6 milionu naplnilo studijní kritéria. Pacienti byli rozděleni do tří skupin: 1. dyslipidemie, 2. LDL-c bez léčby ≥ 3,4 mmol/ l a 3. ischemická choroba srdeční. Průměrný věk účastníků sledování byl 62 let, 50 % tvořily ženy a 11 % černoši. LDL-c byl mezi 2,2– 3,9 mmol/ l. Ve skupině pacientů č. 1 a č. 3 bylo 54 % léčeno standardní hypolipidemickou léčbou, inhibitory PCSK9 byly předepsány < 1 % pacientů, kteří by pro takovou léčbu byli vhodní (obr. 2). Preskripce inhibitorů PCSK9 byla nejvyšší u pacientů s ischemickou chorobou srdeční, a ačkoliv se v čase preskripce zvyšovala, byla stále velmi nízká.
![Trend v proskripci inhibitorů PCSK9 v letech 2015–2017. Upraveno podle [12].](https://www.kardiologickarevue.cz/media/cache/resolve/media_object_image_small/media/image_pdf/1245fee91b325f72c98f4c61adfaea4d.png)
Přitom je léčba inhibitory PCSK9 v reálné praxi srovnatelně účinná tak, jak je tomu ve velkých randomizovaných klinických studiích. Například u pacientů s familiární hypercholesterolemií [13], kteří jsou léčeni inhibitory PCSK9, dosahuje 85,4 % pacientů více než 50% redukce LDL-c nebo hodnoty LDL-c < 2 mmol/ l. To je výrazně lepší výsledek ve srovnání s ostatními pacienty s familiární hypercholesterolemií, kteří nejsou léčeni inhibitory PCSK9, a u kterých jen 50,2 % dosáhne podobného snížení LDL-c (p < 0,001) (obr. 3).
![Změna hodnoty LDL-c v závislosti
na medikaci inhibitory PCSK9. Upraveno
podle [13].](https://www.kardiologickarevue.cz/media/cache/resolve/media_object_image_small/media/image_pdf/88c1cfd096d233fcb274c3b41c655cfd.png)
Podobná situace je v reálné praxi u pacientů s KVO [14]. Konvenční hypolipidemická léčba vede ke snížení LDL-c o cca 38 %. U více než 50 % pacientů neumožňuje ale dosažení cílových hodnot 1,8 mmol/ l. Pomocí léčby inhibitory PCSK9 lze dosáhnout i v reálné praxi snížení LDL-c o dalších 54 % a tím zvýšit počet pacientů dosahujících cílové hodnoty o 42 % (obr. 4).
![Průměrná koncentrace LDL-c v závislosti na léčbě hypolipidemiky u pacientů s kardiovaskulárním onemocněním. Upraveno podle [14].](https://www.kardiologickarevue.cz/media/cache/resolve/media_object_image_small/media/image_pdf/3dcd7e2bd7a3d52ce8cf42b57b030353.png)
Kazuistika 1
Pacient v sekundární prevenci po prodělaném akutním IM, s familiární hypercholesterolemií
Pacient, nar. 1979, se dostavil na vyšetření do naší ambulance pro poruchy metabolizmu lipidů po prodělaném akutním IM, s významnou hypercholesterolemií, k vyšetření a doporučení dalšího postupu v léčbě hypercholesterolemie.
Rodinná anamnéza
Otec zemřel náhle ve věku 51 let na zástavu srdce v.s. (náhlá srdeční smrt doma), léčil se s diabetes mellitus (DM). Bratr – DM, 2. bratr – bez DM. Matka otce – DM nad 60 let. Matka 56 let – IM 0, CMP 0, má onemocnění srdce (chlopně) a byla na operaci a má hypercholesterolemii – předepsaná hypolipidemika. Otec matky hypercholesterolemie, zemřel ve věku 65 let na zástavu srdce, měl DM, a jeho bratr měl rovněž DM. Matka matky zemřela, žlučník. Bratr 38 let – prodělal IM ve věku 34 let, je po aortokoronárním bypassu v 2/ 2015. Sestra 26 let – léčí se s hypercholesterolemií a má hypolipidemika (Inegy 10/ 10). Tři děti – dvojčata 10 let – cholesterol vysoký, užívají „písek“, dcera 7 let – norm. cholesterol.
Alergie neguje, ex kuřák, alkohol příležitostně. Pracovní a sociální anamnéza – řidič kamionu, ženatý.
Medikace – Godasal 100 mg 0-1-0, Tritace 2,5 mg 1-0-0, Sorvasta 40 MG 0-0-1, Siofor 1 000 mg 1-0-1, Januvia 100 mg 1-0-0, Concor 5 mg 1-0-0, Trombex 75 mg 1-0-0 do 10/ 15.
Objektivní anamnéza
Stav po OPCAB LIMA-RIA RIMA-LMS1 10/ 14.
Ischemická choroba srdeční:
- akutní IM spodní stěny a laterálně (4. 10. 2014),
- fibrilace komor v úvodu, KPCR (celkem 20 min),
- UPV 4. 10. až 10. 10. 2014,
- respirační insuficience, plicní edém (7. 10. 2014),
- uzávěr ACD proximálně (kolat. z RIA), uzávěr RMS1, RPLS 50 % stenóza kmene ACS, dlouhá 60% stenóza RIA, 50% stenóza perif. RIA (SKG 17. 10. 2014),
- akineza až dyskineza apikální 1/ 2 spodní, zadní a bočné stěny (UZ 10/ 14), ejekční frakce LK 45 % (UZ 10/ 14).
AV insuficience méně významné (UZ 10/ 14).
DM 2. typu (PAD) od 4/ 14.
Hypercholesterolemie.
Subj.: stenokardie O, spíše bolesti jizvy po sternotomii, dušnost O, močení a stolice bez obtíží.
Obj.: váha 102 kg, výška 183 cm, TK vsedě 110/ 50 po 5 min v klidu, TF 67/ min. Status praesens – pacient při vědomí, orientovaný, chodící, bez klidové dušnosti, ikteru či cyanózy, přiměřené hydratace, nadváha. Nejsou xantelezmata víček, nejsou xantomy. Kůže s normálním nálezem. Muskuloskeletální systém s normálním nálezem. Hlava – zornice izokorické, spojivky prokrvené, jazyk vlhký, nepovleklý, plazí ve střední čáře. Krk – pulzace karotid symetrická, bez šelestu, není zvýšená náplň krčních žil, štítnou žlázu ani uzlinový syndrom nehmatám. Hrudník – jizva po sternotomii, symetrický, poklep plný jasný, dýchání čisté, sklípkové, v celém rozsahu, AS pravidelná, 70/ min, ozvy 2, ohraničené, šelest neslyším, není akcentace 2. ozvy nad aortou. Břicho v úrovni, jizvy O, měkké, prohmatné, není peritoneální, bez hmatné rezistence, není hepatosplenomegalie. Játra s obloukem v MCL čáře. Končetiny – horní končetiny s normálním nálezem, dolní končetiny bez otoků, bez známek zánětu, pulzace hmatné do periferie. Neurologicky orientačně bez lateralizace.
Výsledky laboratorních vyšetření a průběh léčby hypercholesterolemie (tab. 1).
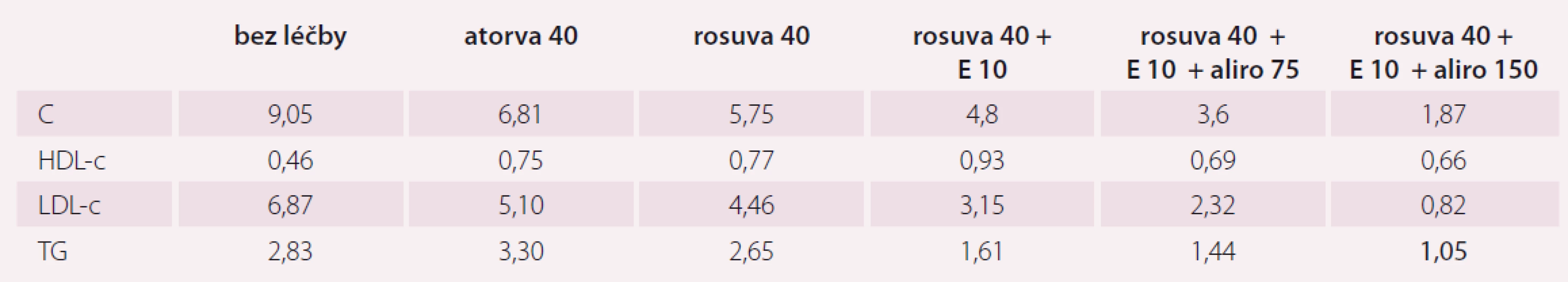
Kazuistika 2
Pacient v sekundární prevenci po prodělaném akutním IM, netolerující léčbu statiny pro myalgie
Pacient, nar. 1961, dostavil se na vyšetření do ambulance pro poruchy metabolizmu lipidů po prodělaném akutním IM, s významnou hypercholesterolemií, k vyšetření a doporučení dalšího postupu v léčbě hypercholesterolemie. V anamnéze je přítomna intolerance všech dostupných statinů (atorvastatin, rosuvastatin, simvastatin, fluvastatin) z důvodu myalgií, ustupujících po vysazení léčby statiny.
Rodinná anamnéza
Otec měl IM v 38 letech, HLP, hypertenze, zemřel v 88 letech. Matka – HLP, kloubní postižení. Sourozenci – bratr a sestra s HLP, syn astma bronchiale, HLP.
Objektivní anamnéza
Ischemická choroba srdeční:
- pozitivní ergometrie 02/ 2017,
- nemoc 3 tepen (KG 03/ 2017),
- normální systolická funkce a kinetika LK (UZ 02/ 2017), EF 70 %, diastolická dysfunkce LK,
- stav po chirurgické revaskularizaci myokardu 27. 04. 2017 (ECC: LIMA-RIA, Y-graft (LIMA)-RIMA-RMS).
AV insuficience málo významné 1/ 4 (UZ 02/ 2017).
Familiární hypercholesterolemie:
- intolerance statinů (atorvastatin, rosuvastatin, simvastatin, fluvastatin) pro myalgie, ustupující po vysazení statinu
Stav po renální kolice s dilatací dutého systému vlevo:
- stav po extrakci konkrementu vlevo 11/ 2015.
Gonartróza vlevo.
Stav po hepatitidě A v dětství.
Stav po hemilaminektomii L5 vpravo a dekompresi L5, S1 r. 2009.
Stav po operaci levého kolene pro úraz 1991.
Stav po ASK pravého kolenního kloubu 2016.
Medikace – Ezetrol 10 mg 1 × 1 tbl., Godasal 100 mg 1 × 1 tbl., Concor Cor 2,5 mg 0,5 × 1 tbl., Tritace 2,5 mg 0,5 × 1 tbl.
Alergie neudává, sociální a pracovní anamnéza – ženatý, manažer u hasičů. Ex kuřák, alkohol příležitostně.
Subj.: neguje dušnost či stenokardie, stolice a močení norm.
Obj.: výška 186 cm, váha 123,0 kg, TF 65/ min, TK 140/ 80 LHK po 5 min v klidu. Pacient při vědomí, orientovaný, chodící, bez klidové dušnosti, ikteru či cyanózy, přiměřené hydratace. Není arcus lipoides cornae, nejsou šlachové ani kožní xantomy. Zornice isokorické, reagující, hrdlo klidné, jazyk vlhký, chrup sanován. Pulsace ACC symetrické, bez šelestu, náplň krč. žil nezvětšena, štítná žláza nehmatná, dýchání sklípkové čisté, AS pravidelná, ozvy 2, ohraničené, břicho – játra ani slezina nehmatná, bez patologické resistence, lýtka bez známek flebitidy, pulzace tepen do periferie dobře hmatné. Není zevní uzlinový syndrom. Neurologicky orientačně bez lateralizace (tab. 2).
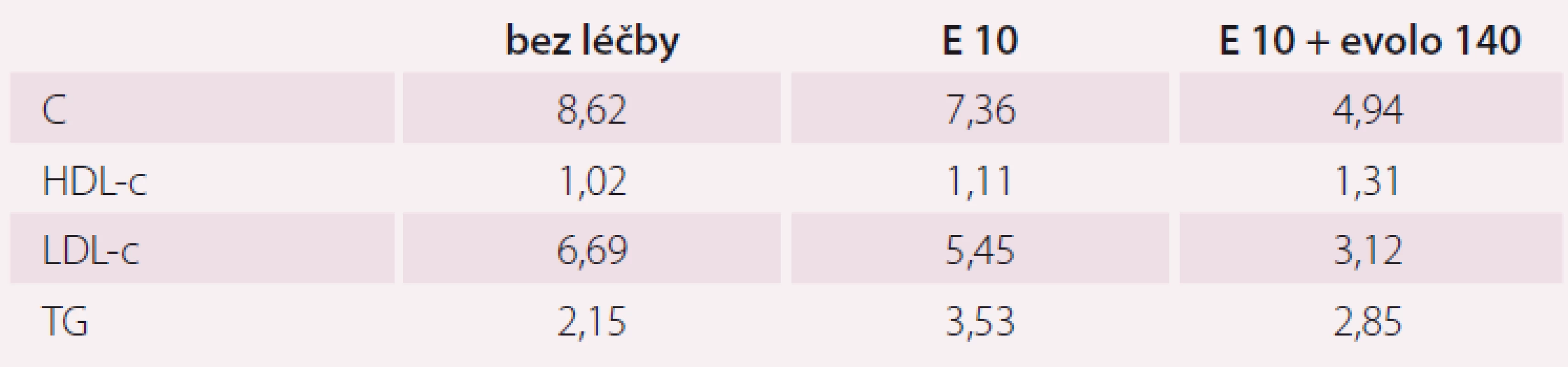
Komentář
Pacient v naší první kazuistice je léčen v rámci sekundární prevence po prodělaném akutním IM, navíc v kombinaci s familiární hypercholesterolemií. Pro přetrvávající neuspokojivě kompenzovaný lipidogram při současném nedosažení cílových hodnot LDL-c byla do jeho léčby zařazena kombinace hypolipidemik. Teprve při kombinaci s inhibitorem PCSK9 došlo k dosažení cílových hodnot.
Druhý pacient v kazuistice je léčen v rámci sekundární prevence po chirurgické revaskularizaci myokardu a současné familiární hypercholesterolemii. Je prototypem pacienta s myopatií, asociovanou s léčbou statiny (SAMS = statin-associated muscle symptoms). U tohoto typu nemocných bylo dosud velmi obtížné dosáhnout cílových hodnot LDL-c, nebo se k nim alespoň přiblížit. Léčba inhibitorem PCKS9 vedla v tomto případě ke snížení LDL-c o více než 50 %, tudíž k naplnění cílových hodnot.
Závěr
V léčbě pacientů s hypercholesterolemií nám v klinické praxi jde nejenom o dosažení cílových hodnot LDL cholesterolemie, ale vždy především o snížení KV rizika, které plyne z akcentované aterogeneze vlivem vysoké hodnoty LDL-c. U některých pacientů je nutné k dosažení tohoto cíle použít individualizovaný přístup, protože standardní léčba hypolipidemiky typu statinů či ezetimibu není dostatečně účinná, nebo ji pacienti netolerují – zejména z důvodu myopatie asociované s léčbou statiny. Nové typy hypolipidemik jako jsou inhibitory PCKS9 mají u takových pacientů velmi slibný potenciál pro využití v klinické praxi.
Práce byla podporována výzkumnými projekty AZV ČR č. 17-31754A, Progres Q40 LF UK Hradec Králové
Doručeno do redakce: 29. 6. 2019
Přijato po recenzi: 9. 7. 2019
prof. MU Dr. Vladimír Blaha, CSc.
Zdroje
1. Stone NJ, Robinson JG, Lichtenstein AH et al. 2013 ACC/ AHA guideline on the treatment of blood cholesterol to reduce atherosclerotic cardiovascular risk in adults: a report of the American College of Cardiology/ American Heart Association Task Force on Practice Guidelines. Circulation 2014; 129 (25 Suppl 2): S1– S45. doi: 10.1161/ 01.cir.0000437738.63853.7a.
2. Gitt AK, Lautsch D, Ferrieres J et al. Low-density lipoprotein cholesterol in a global cohort of 57,885 statin-treated patients. Atherosclerosis 2016; 255: 200– 209. doi: 10.1016/ j.atherosclerosis.2016.09.004.
3. Piepoli MF, Hoes AW, Agewall S et al. 2016 European Guidelines on cardiovascular disease prevention in clinical practice: the Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice. Atherosclerosis 2016; 252: 207– 274. doi: 10.1016/ j.atherosclerosis.2016.05.037.
4. Catapano AL, Graham I, De Backer G et al. 2016 ESC/ EAS guidelines for the management of dyslipidaemias. Eur Heart J 2016; 37(39): 2999– 3058. doi: 10.1093/ eurheartj/ ehw272.
5. REPATHA® (evolocumab) prescribing information. Thousand Oaks, CA: Amgen Inc; 2016. Available at: https:/ / www.pi.amgen.com/ ~/ media/ amgen/ repositorysites/ pi-amgen-com/ repatha/ repatha_pi_hcp_english.pdf.
6. PRALUENT® (alirocumab) prescribing information. Bridgewater, NJ: Sanofi-Aventis; 2017. Available at: ttps:/ / www.accessdata.fda.gov/ drugsatfda_docs/ label/ 2017/ 125559s002lbl.pdf
7. Koren MJ, Sabatine MS, Giugliano RP et al. Long-term low-density lipoprotein cholesterol-lowering efficacy, persistence, and safety of evolocumab in treatment of hypercholesterolemia: results up to 4 years from the open-label OSLER-1 extension study. JAMA Cardiol 2017; 2(6): 598– 607. doi: 10.1001/ jamacardio.2017.0747.
8. Hirayama A, Yamashita S, Ruzza A et al. Long-term treatment with evolocumab among japanese patients – final report of the OSLER open-label extension studies. Circ J 2019; 83(5): 971– 977. doi: 10.1253/ circj.CJ-19-0139.
9. Sabatine MS, Giugliano RP, Keech AC et al. Evolocumab and clinical outcomes in patients with cardiovascular disease. N Engl J Med 2017; 376(18): 1713– 1722. doi: 10.1056/ NEJMoa1615664.
10. Schwartz GG, Steg PG, Szarek M et al. Alirocumab and cardiovascular outcomes after acute coronary syndrome. N Engl J Med 2018; 379(22): 2097– 2107. doi: 10.1056/ NEJMoa1801174.
11. Giugliano RP, Keech A, Murphy SA et al. Clinical efficacy and safety of evolocumab in high-risk patients receiving a statin: secondary analysis of patients with low LDL cholesterol levels and in those already receiving a maximal-potency statin in a randomized clinical trial. JAMA Cardiol 2017; 2(12): 1385– 1391. doi: 10.1001/ jamacardio.2017.3944.
12. Chamberlain AM, Gong Y, Shaw KM et al. pcsk9 inhibitor use in the real world: data from the National Patient-Centered Research Network. J Am Heart Assoc 2019; 8(9): e011246. doi: 10.1161/ JAHA.118.011246.
13. Razek O, Cermakova L, Armani H et al. Attainment of recommended lipid targets in patients with familial hypercholesterolemia: real-world experience with PCSK9 inhibitors. Can J Cardiol 2018; 34(8): 1004– 1009. doi: 10.1016/ j.cjca.2018.04.014.
14. Saborowski M, Dölle M, Manns MP et al. Lipid--lowering therapy with PCSK9-inhibitors in the management of cardiovascular high-risk patients: Effectiveness, therapy adherence and safety in a real world cohort. Cardiol J 2018; 25(1): 32– 41. doi: 10.5603/ CJ.a2017.0137.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2019 Číslo 3
Nejčtenější v tomto čísle
- Kardiovaskulární působení rekreačních drog (kokain, marihuana, metamfetamin)
- Sarkoidóza – aktuální pohled na patogenezi, diagnostiku a léčbu
- Epidemiologie tuberkulózy
- PCSK9 inhibitory v klinické praxi – update
