Klinické studie ukončené, přednesené nebo publikované v poslední době
Autoři:
prof. MUDr. Jindřich Špinar, CSc.; Fesc 1; Prof. MUDr. Jiří Vítovec, CSc.; Fesc 2; MUDr. Jiří Pařenica 1; MUDr. Tomáš Brychta 1
Působiště autorů:
Interní kardiologická klinika FN Brno-Bohunice
1; 1. interní kardioangiologická klinika FN u sv. Anny
2
Vyšlo v časopise:
Kardiol Rev Int Med 2005, 7(4): 205-210
Kategorie:
Klinické studie
Uvádíme klinické studie prezentované na kongresu European Society of Cardiology 3.-7. 9. 2005 ve Stockholmu a na American Heart Association 13.-16. 11 2005 v Dallasu, Texas. Některé z nich byly souběžně publikovány in extenso.
ASCOT BPLA (Anglo-Scandinavian Cardiac Outcomes Trial)
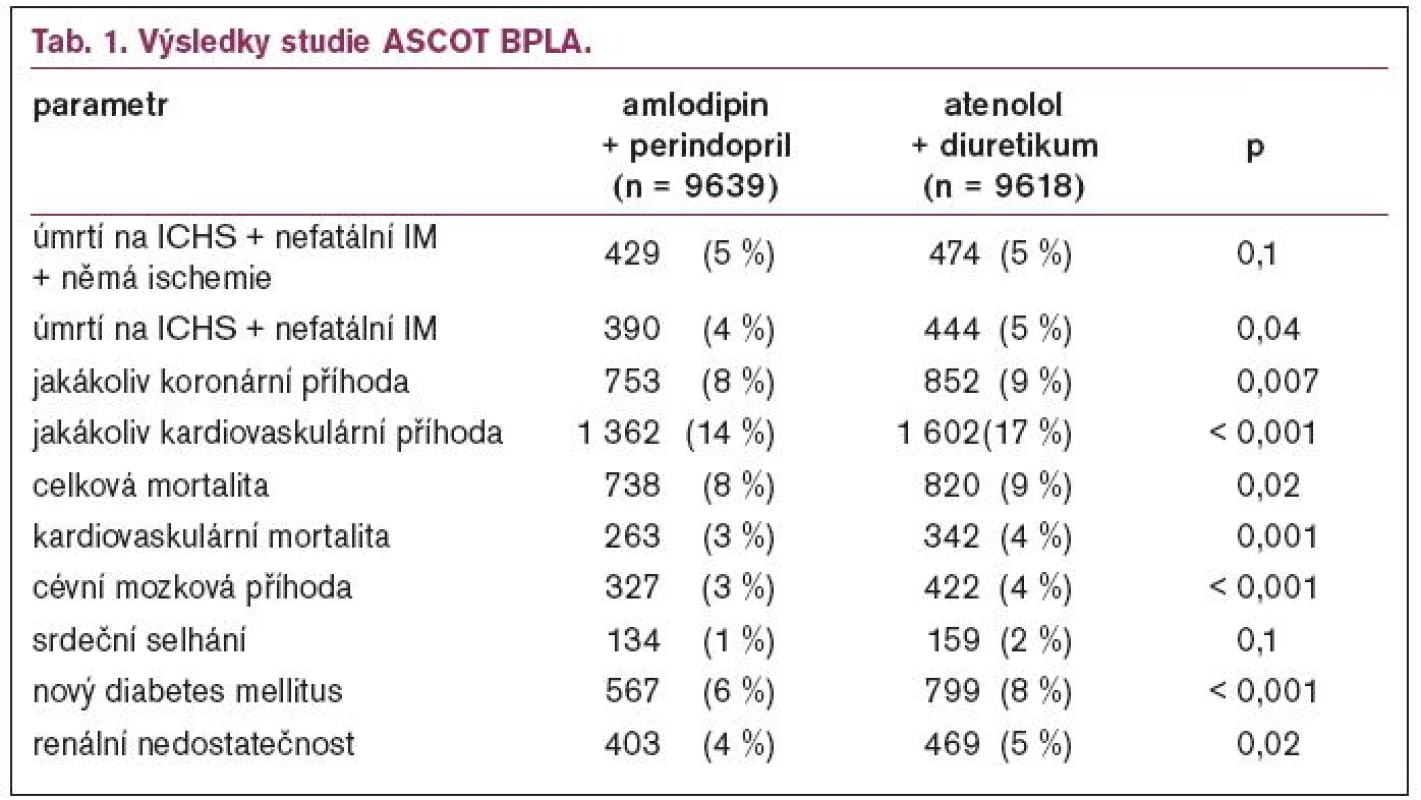
ASCOT BPLA (Anglo-Scandinavian Cardiac Outcomes Trial) byla ve Stockholmu přednesena s kompletními výsledky (předběžné byly již na jaře 2005) a současně byla i publikována v Lancetu. Studie zařadila 19 257 hypertoniků ve věku 40-79 let, kteří museli mít více rizikových faktorů. U poloviny nemocných (n = 9639) byla léčba zahájena amlodipinem 5 mg u druhé poloviny (n = 9618) atenololem 50 mg. Pokud nebyla dostatečná kontrola krevního tlaku, byl amlodipin zvýšen na 10 mg a atenolol na 100 mg, pokud nadále nebyla dobrá kontrola tlaku, byl k amlodipinu přidán perindopril (4-8 mg) a k atenololu bendroflumethiazid (1,25-2,5 mg). Kombinaci amlodipin + perindopril mělo 49,5 % nemocných v 1. větvi a kombinaci atenolol + diuretikum 54,9 % nemocných v 2. větvi. Průměrná doba sledování byla 5,5 let, což je v součtu všech nemocných 106 153 pacientských let. Studie byla ukončena předčasně pro jasný prospěch z léčby ve větvi amlodipin + perindopril. Hlavní výsledky studie ukazuje tab. 1.
Průměrný krevní tlak byl 164,0/94,7 mmHg na začátku studie a poklesl na 136,9/78,3 mmHg. U nemocných léčených amlodipinem nebo kombinací amlodipin + perindopril byl průměrný krevní tlak v průběhu studie o 2,7/1,9 mmHg nižší, na konci studie byl tlak na v této větvi 136,1/77,4 mmHg a ve větvi atenololové 137,7/79,2 mmHg. Vzhledem k tomu, že na základě studie HOT víme, že pokles pod 138/83 mmHg již nepřináší další prospěch, je jasné, že rozdíly v krevním tlaku nemohly ovlivnit výsledky studie.
Dodatečná analýza podskupin nezjistila větší rozdíly ve výsledku podle pohlaví, věku či přítomnosti doprovodných onemocnění (diabetes, renální insuficience) a větší prospěch z léčby založené na amlodipinu a perindoprilu byl výrazný ve všech podskupinách.
Na kongresu American Heart Association v Dallasu byly prezentovány výsledky podstudie Conduit Artery Function Evaluation (CAFE) u 2 199 nemocných ze studie ASCOT. Centrální krevní tlak byl měřen neinvazivně přístrojem Sphygmocor a porovnáván s tlakem brachiálním. Přestože tlaky brachiální se nelišily, tak centrální systolický krevní tlak byl snížen v amlodipinové větvi o 4,3 mmHg více a centrální pulzní tlak o 3,0 mmHg více než u nemocných léčených betablokátorem.
Literatura
Dahlof B for the ASCOT investigators. Prevention of coronary stroke events with an antihypertensive regimen of amlodipin adding perindopril as required versus atenolol adding bendroflumethiazide as reguired, in the Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BPLA): a multicentre randomised controlled trial. Lancet 2005; 366: 895-906.
Poulter NR fot the ASCOT investigators. Role of blood pressure and other variables in the differential cardiovascular event rate noted in the the Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BPLA). Lancet 2005; 366: 907-13.

PREAMI (Perindopril Remodelling in Elderly with Acute Myocardial Infarction)
Další velkou, ukončenou a prezentovanou klinickou studií s pozitivním výsledkem byla studie PREAMI (Perindopril Remodelling in Elderly with Acute Myocardial Infarction) která si položila dotaz, zda má smysl podávat ACE-inhibitor (perindopril) starším nemocným časně po infarktu myokardu, i když mají dobrou funkci levé komory srdeční. Studie PREAMI si kromě klasických cílů – mortalita a morbidita – všímala především echokardiografických nálezů, především enddiastolického objemu levé komory a jeho změny po infarktu myokardu. Do studie byli zařazeni nemocní časně po infarktu myokardu starší 65 let a s ejekční frakcí > 40 %. Nesměli mít projev závažného srdečního selhání (klidovou dušnost) a laboratorní známky renální insuficience. Museli mít dobrou echokardiografickou vyšetřitelnost a předchozí léčba ACE-I byla ukončena > 24 hodin před zařazením. Perindopril byl titrován od 4 do 8 mg, studie byla naplánována na 12 měsíců.
Do studie bylo zařazeno 1 252 nemocných ve 109 centrech v 5 zemích. Průměrný věk byl 73 let a randomizace musela být provedena do 20 dnů od akutního infarktu myokardu (průměr byl 11 dní). V aktivní větvi s perindoprilem bylo zařazeno 631 nemocných, žádný se v průběhu sledování neztratil a konečné vyhodnocení bylo provedeno u 455 nemocných, u 121 nemocných bylo echokardiografické vyšetření nekvalitní nebo nebylo neprovedeno. V placebové větvi bylo 621 nemocných, 2 se v průběhu studie ztratili a dostatečně kvalitní echo vyšetření na začátku i na konci studie bylo u 441 nemocných. Průměrný konečný diastolický objem levé komory na začátku studie byl 81,3 ml v aktivní větvi a 79,3 ml v placebové, konečný systolický 34,2 ml resp. 33,1 % a ejekční frakce 58,9 % resp. 59,3 %, průměrný krevní tlak byl 126/74 mmHg resp. 125/74 mmHg (vše ns).
Výskyt úmrtí, srdečního selhání a negativní remodelace (vzestup EDV > 8 %) – primární cíl – byl u nemocných léčených perindoprilem snížen o 38 % (p < 0,001), počet úmrtí se nelišil, počet hospitalizací pro srdeční selhání klesl o 27 % (p = 0,24). Konečný diastolický objem stoupl o 8 % a více u 27,7 % nemocných léčených perindoprilem a u 51,2 % léčených placebem (snížení rizika o 46 %, p < 0,001). Konečný diastolický objem na placebu na konci studie byl 83,6 ml a na aktivní léčbě 81,8 ml (p < 0,01).
Negativní remodelace byla ve stejné míře snížena u mužů i žen (63 resp. 65 %), mladších i starších 73 let (65 resp. 61 %), hypertoniků i nehypertoniků (60 resp. 69 %), na hypolipidemicích i bez nich (44 resp. 29 %), na betablokátorech i bez nich (35 resp. 39 %).
Studie jasně prokázala, že i u starších nemocných s malou levou komorou srdeční a dobrou systolickou funkcí po čerstvém infarktu myokardu je perindopril nejen výborně tolerován, ale dokáže zabránit nežádoucí remodelaci, respektive dilataci levé komory. V celé studii pouze 1,6 % nemocných léčených perindoprilem mělo suchý kašel. Nebyl zaznamenán vyšší výskyt nežádoucí hypotenze, přestože výchozí TK byl v průměru o 15 mmHg pod hranicí normotenze.
Studie PREAMI je svými výsledky plně v souladu s výsledky studie EUROPA a HOPE, kde po 1. roce taktéž nebyl rozdíl v mortalitě mezi léčenou a placebovou větví, ale začínal se objevovat trend ve zlepšení kvality života, měřené např. počtem hospitalizací pro srdeční selhání.
FIELD (Fenofibrate Intervention and Event Lowering in Diabetes)
Ve studii bylo randomizováno 9 795 diabetiků ve věku 50-75 let, s cholesterolem 3,0-6,5 mmol/l a s triglyceridy 1,0-5,0 mmol/l na léčbu fenofibrátem (200 mg) nebo placebem. Všem byla doporučena dietní opatření. Vylučovacím kritériem byla např. léčba jiným hypolipidemikem, nebo renální nedostatečnost (kreatinin > 130 mmol/l). Mezi randomizovanými převažovali nemocní se neznámou ICHS (n = 7683) a muži (n = 6 139). Studie probíhala v Austrálii, na Novém Zélandě a ve Finsku.

Na začátku studie byla 4týdenní úvodní fáze s dietními opatřeními následovaná 6týdenní fází jednoduše zaslepené placebem. Pokud nemocní neměli kardiovaskulární příhodu, následovala 6týdenní zaslepená fáze s 200 mg fenofibrátu denně. Pokud nemocní ani po této fázi neměli kardiovaskulární příhodu, byli randomizováni na léčbu 200 mg mikronizovaného fenofibrátu nebo odpovídající kapsli placeba.
Na začátku studie nesměli být nemocní léčeni statinem. V průběhu studie, kdy se objevily další pozitivní důkazy pro statiny, směly být tyto do léčby přidány, a tak na konci studie 36 % nemocných v placebové větvi a 19 % ve fibrátové větvi mělo statin (p < 0,001).
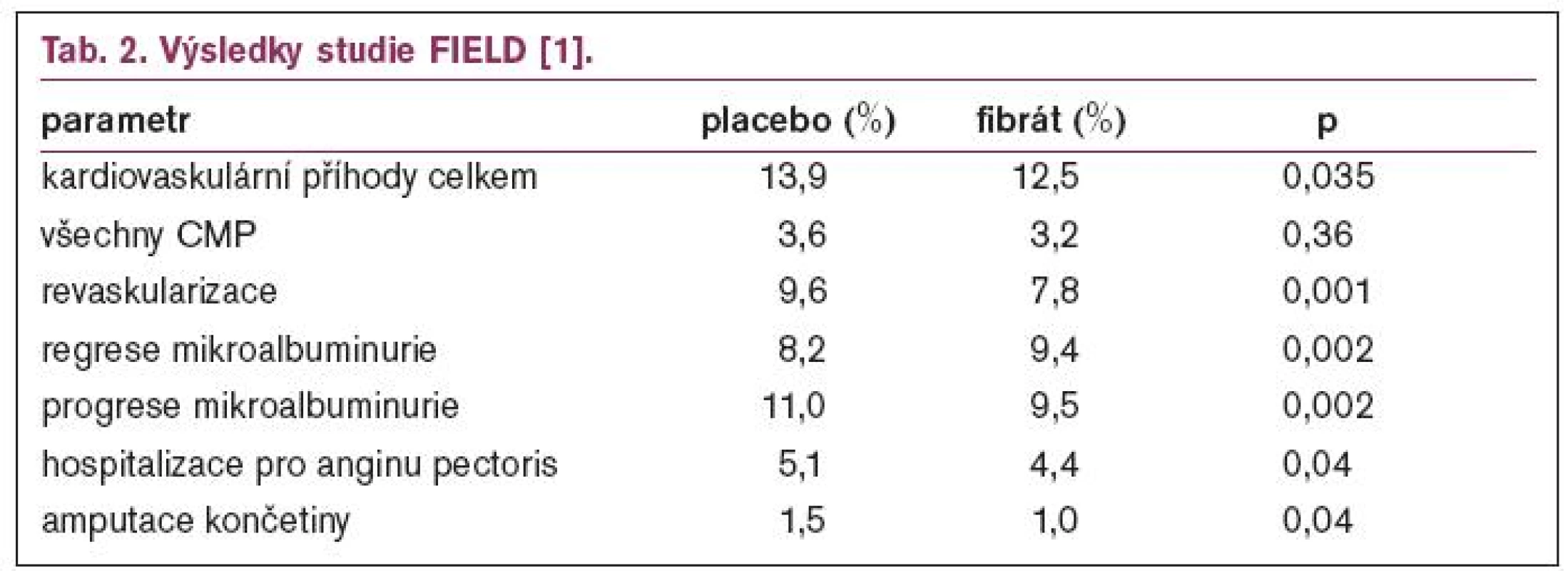
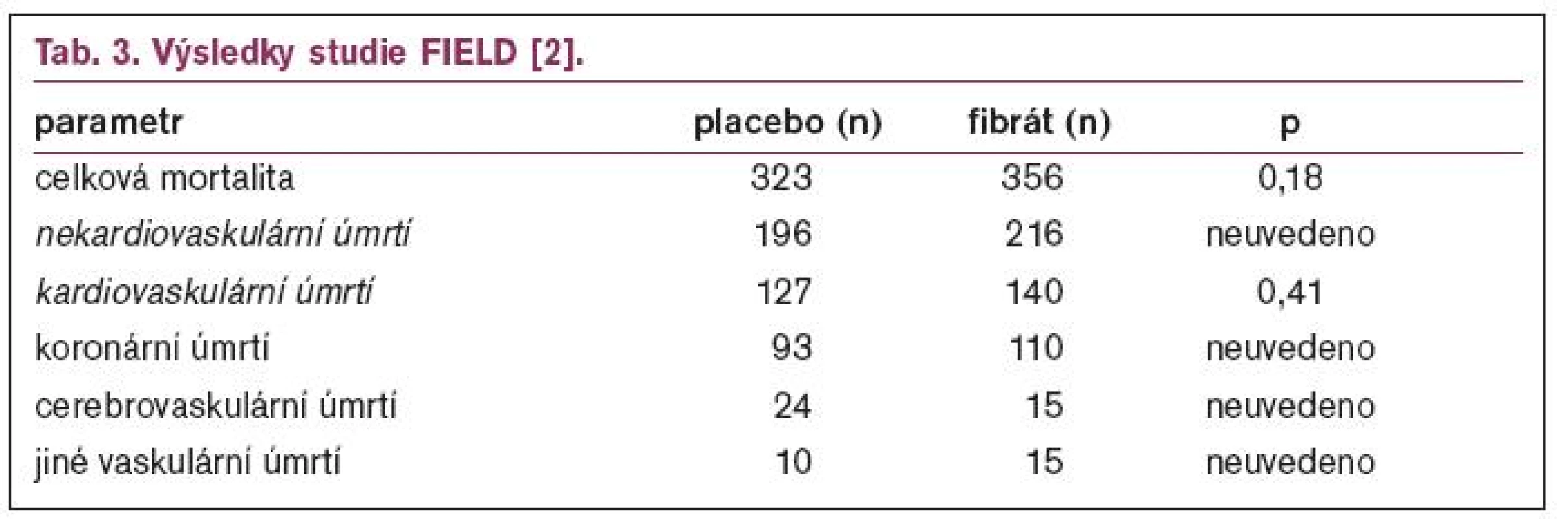
Výsledky studie FIELD ukazuje tab. 2 a 3.
Studie FIELD neprokázala snížení celkové ani kardiovaskulární mortality u diabetiků léčbou fenofibrátem. Při retrospektivní analýze dospěli autoři k závěru, že hlavní příčinou byl téměř dvojnásobný počet nemocných léčených statinem v průběhu studie v placebové větvi, oproti větvi s aktivní léčbou. Proto také rozdíly v lipidovém spektru, které byly významné po prvních 4 měsících léčby, byly poměrně malé na konci studie. Při analýze podskupin byl větší efekt fenofibrátu na primární cíl pozorován u nemocných bez známé ischemické choroby srdeční a u nemocných s nízkým HDL-cholesterolem. Jako zásadní ponaučení z této studie vyplývá, že léčba fibráty je velmi bezpečná, počet nežádoucích účinků byl srovnatelný s placebem, nenahrazuje však léčbu statiny. Budeme-li na diabetiky pohlížet jako na nemocné v sekundární prevenci nebo alespoň jako na nemocné s vysokým kardiovaskulárním rizikem, pak základem léčby by mělo být dosažení cílových hodnot cholesterolu především pomocí statinu, ke kterému u diabetické dyslipidemie přidáme fibrát.
Literatura
The FIELD investigators. The need for a large-scale trial of fibrate therapy in diabetes: the rationale, design of the Fenofibrate Intervention and Event Lowering in Diabetes (FIELD study). Cardiovascular diabetology 2004; 3: 9-20.
The Field study investigators. Effects of long term fenofibrate therapy on cardiovascular events in 9795 people with type 2 diabetes mellitus (the FIELD study): randomised controlled trial. Lancet 2005; v tisku.
The Incremental Decrease in Clinical Endpoints Through Aggressive Lipid Lowering (IDEAL) Trial
Studie IDEAL byla přednesena v Dallasu v sekci HOT lines a současně publikována v časopise JAMA. Studie měla podobná vstupní kritéria jako dnes již historická první mortalitní studie se statiny – 4S, jejíž výsledky byly poprvé předneseny ve stejném sále – Arena Dallas Conventional Centrum – v roce 1994.
Studie zahrnula 8 888 nemocných (přesně 2krát více než studie 4S, která měla 4 444 nemocných), kteří byli indikováni k léčbě statiny. Mezi vylučovacími kritérii byly triglycerid < 6,8 mmol/l a léčba statinem v dávce větší než 20 mg simvastatinu (nebo ekvivalent jiného statinu). Léčba byla otevřená, medikace byla psána na recepty. Celkem 4 449 nemocných dostalo simvastatin 20 mg, který mohl být zvýšen na 40 mg, a 4 438 nemocných dostalo atorvastatin v dávce 80 mg (tzv. PROBE design – Prospective Randomised Open label Blind Evaluation).
Průměrný věk nemocných byl 61,6 let, 81 % byli muži, 12 % diabetici, 33 % hypertonici, 40 % bylo po CABG nebo PTCA a 75 % bylo před zařazením léčeno statinem, 50 % simavastatinem a 12 % atorvastinem.
Nemocní léčení simvastatinem měli průměrný LDL-cholesterol v průběhu studie 2,7 mmol, HDL 1,22 mmol, pokles oproti výchozí hodnotě u LDL-cholesterolu byl 33% u nemocných neléčených statiny a 5% u nemocných léčených statiny. Nemocní léčení atorvastatinem měli průměrný LDL-cholesterol v průběhu studie 2,1 mmol, HDL 1,19 mmol, pokles oproti výchozí hodnotě u LDL cholesterolu byl 47% u nemocných neléčených statiny a 27% u nemocných léčených statiny.
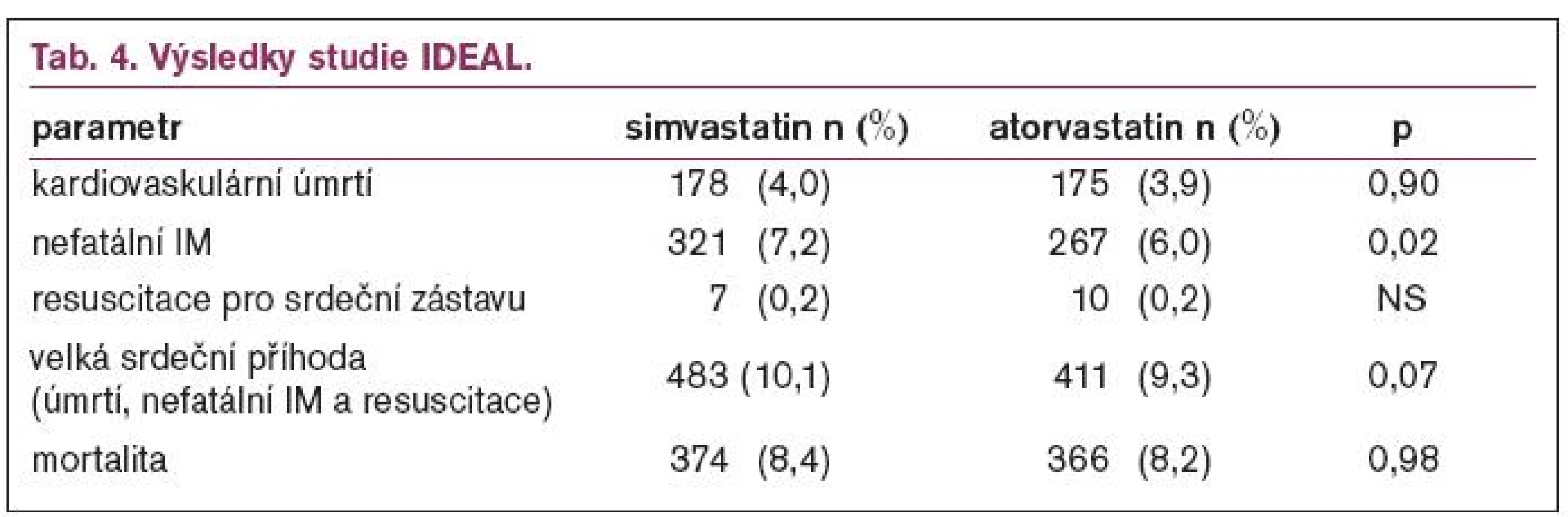
Výsledky studie IDEAL ukazuje tab. 4.
Z tabulky je patrné, že celková ani kardiovaskulární mortalita nebyly ovlivněny, statisticky významně byl snížen počet nefatálních infarktů myokardu. Z vedlejších cílů bylo zajímavé významné snížení počtu revaskularizací u nemocných léčených atorvastatinem (< 0,0001). Velmi důležité jsou poznatky o bezpečnosti léčby, kdy počet rabdomyolýz byl 5 (3krát simva, 2krát atorva) a počet vyřazení pro nežádoucí účinky byl 92 (41 simva a 51 atorva), což ukazuje na bezpečnost léčby vysokými dávkami statinů.
Literatura
The IDEAL investigators. High dose Atorvastain versus usual dose Simvastatin in Secondary Prevention after Myocardial Infarction. The Incremental Decrease in Clinical Endpoints Through Aggressive Lipid Lowering (IDEAL) Trial. JAMA 2005; v tisku.
ACTIVE W
Cílem studie ACTIVE je vyhodnotit kombinovanou antiagregační léčbu klopidogrelem + ASA u pacientů s fibrilací síní. V rameni ACTIVE W je tato léčbu srovnávána s warfarinem, v rameni ACTIVE A se samotnou ASA. Souběžně je v obou větvích u pacientů, kteří nemají kontraindikaci léčby irbesartnem, sledován efekt léčby irbesartanem 300 mg/den oproti placebu (ACTIVE I).
Vstupním kritériem je dokumentovaná fibrilace síní (paroxyzmální – alespoň 2 ataky v odstupu 14 dnů, perzistentní, permanentní) plus alespoň 1 další rizikový faktor (hypertenze, věk ≥ 75 let, předchozí CMP/TIA, LVEF < 45 %, ICHDKK nebo ve věk 55-74 let ICHS nebo diabetes mellitus). Plánováno bylo zařazení 6 500 pacientů do větve W, 7 500 pacientů do větve A.
Rameno ACTIVE W bylo předčasně ukončeno pro průkaz superiority perorální antikoagulační léčby, výsledky byly prezentovány na AHA v Dallasu. Větev ACTIVE A a ACTIVE I dále pokračuje.
V rameni W je srovnáván klopidogrel 75 mg + ASA 100 mg nebo warfarin (cílová hodnota INR 2-3). Primární sledovaný cíl je výskyt CMP, systémové embolizace non-CNS, IM, vaskulární úmrtí, sekundární sledovaný cíl je výskyt závažných krvácení.
Studie byla koncipována na průkaz non-inferiority léčby klopidogrelem + ASA oproti warfarinu. Celkem bylo zařazeno 6 706 pacientů z 522 center v 31 zemích (v České republice bylo zařazeno 233 pacientů), 3 371 léčených perorální antikoagulační léčbou, 3 335 léčených klopidogrelem + ASA, skupiny byly srovnatelné co do rizikovosti pacientů (údaje jsou uvedeny v procentech ve skupině léčené antikoagulační terapií vs klopidogrel + ASA - věk ≥ 75 let: 35,4 % vs 34,5 %, LVEF < 45 %: 16,9 % vs 16,5 %, hypertenze 81,5 % vs 81,2 %, předchozí TIA/CMP 15,2 % vs 14,8 %, ICHDKK 3 % vs 2,9 %, věk 54-75 let s dokumentovanou ICHS nebo DM 25,2 % vs 25,1 %). Před vstupem do studie užívalo antikoagulační léčbu 78 % resp 75,7 % pacientů, ASA 28,2 % resp 30,1 % pacientů a klopidogrel 2,3 % resp. 2,6 % pacientů. INR v rozmezí 2-3 bylo dosaženo u 63,9 % pacient-měsíců, INR < 2 v 20,8 % a INR > 3 v 15,4 %. Ve skupině pacientů, kteří při vstupu do studie byli nastaveni na OAC, přerušilo léčbu klopidogrelem + ASA více pacientů (13,4 % vs 6,1 %), ve skupině pacientů, kteří dříve neužívali OAC, bylo přerušení léčby srovnatelné (13,2 % vs 12,4 %).
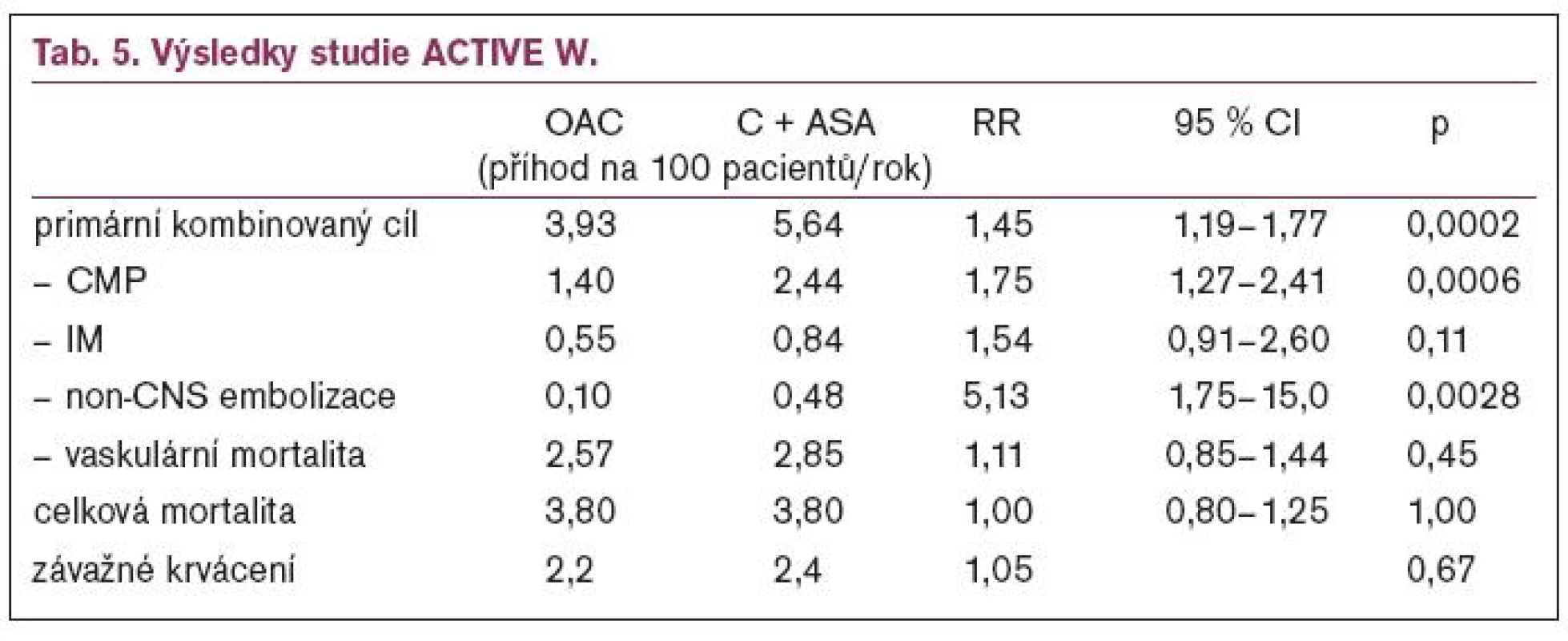
Výsledky studie ACTIVE W ukazuje tab. 5.
V podskupině pacientů, kteří byli při vstupu do studie na OAC, byl významně nižší výskyt kombinovaného primárního cíle (RR 1,5; p = 0,0006), ve skupině, která před vstupem neužívala OAC byl pouze nevýznamný trend ve prospěch OAC (RR 1,32; p = 0,17), ale byl nevýznamný trend k vyššímu výskytu závažných krvácení (RR 0,58, p = 0,09). V centrech, kde bylo INR v doporučeném rozmezí ≥ 65 % pacient-měsíců, byl výskyt primárního cíle u pacientů léčených OAC významně nižší (RR 1,83; p < 0,0001), závažné krvácení bylo častější při léčbě klopidogrel + ASA (RR 1,55; p = 0,027), v centrech s INR v doporučeném rozmezí < 65 % pacient-měsíců byl výskyt primárního cíle srovnatelný (RR 1,11; p = 0,47) a trend k častějšímu krvácení při léčbě OAC (RR = 0,68; p = 0,08).
Závěrem autoři konstatovali, že perorální antikoagulační léčba je u pacientů s fibrilací síní ve srovnání s kombinací klopidogrel + ASA účinnější. Výskyt závažných krvácení je srovnatelný.
REVIVE - Randomized EValuatIons of leVosimEndan
Studie REVIVE se zabývala zhodnocením účinku levosimendanu u akutního srdečního selhání. Vycházela z předpokladu, že v USA je ročně hospitalizováno přes 1milion pacientů s akutním srdečním selháním, z čehož je 70-80 % pacientů s akutním zhoršením chronického srdečního selhání a 20-30 % s nově vzniklým akutním srdečním selháním.
Do studie byli zařazeni pacienti s akutním srdečním selháním s EFLK pod 35 % vyžadující v léčbě podání i.v. diuretika. Byl testován efekt levosiomendanu předaného k plné léčbě srdečního selhání proti placebu. Zařazení pacienti byli rozděleni do 2 studií. Nejprve do pilotní studie – REVIVE I, která měla 100 pacientů a vedla k vytvoření endpointů 2. studie REVIVE II, kde bylo zařazeno 600 pacientů. Do studií bylo zapojeno 103 center ze 3 zemí – USA, Austrálie a Izrael. Po randomizaci byli pacienti rozděleni do 2 skupin a skupina léčená levosimendanem dostala léčbu dle schématu 1 hodinový bolus 6-12 μg/kg/min, dále 6 hodin 0,1 μg/kg/min a do 24hodin tj. 17 hodin 0,2 μg/kg/min.
Výsledky studie byly rozděleny do sledovaných parametrů:
- průběh hodnot B-typu natriuretického peptidu (BNP) v prvních 24 hodinách po podání levosimendanu
- celkový stav pacienta v prvních 6 hodinách
- dušnost v prvních 6 hodinách
- počet dnů života po podání a počet dnů hospitalizace po 14 dnech od podání
- smrt nebo zhoršení srdečního selhání po 31 dnech
- NYHA klasifikace po 5 dnech od podání
- celková mortalita po 90 dnech.
Mezi aktivně léčenou a placebovou skupinou nebyl statistický rozdíl ve sledovaných parametrech (EFLK, léčba, demografické údaje).
Primární cíl REVIVE II složený z výše uvedených parametrů prokázal více zlepšených a méně zhoršených pacientů po levosimendanu na hladině významnosti 0,015 a ještě lepší výsledky při spojeném cíli s REVIVE I na hladině významnosti až 0,0001. Při rozebírání jednotlivých sledovaných parametrů byly lepší výsledky v REVIVE II u 299 pacientů na terapii vs 301 pacientů na placebu především v potřebě celkové léčby srdečního selhání, celkové dušnosti, výskytu plicního edému i dalších sledovaných parametrů. Za léčbu srdečního selhání bylo považováno podání levosimendanu, dobutaminu, neseritidu a milrinonu. Dále byl pozorován významný pokles BNP v 1. a 5. dnu po podání levosimendanu na hladině významnosti 0,001. Délka hospitalizace byla taktéž nižší u pacientů léčených levosimendanem. Z vedlejších účinků levosimendanu byl pozorován vyšší výskyt hypotenze a arytmií - komorových i supraventrikulárních i vyšší výskyt izolovaných komorových extrasystol. Celková mortalita po 90 dnech byla v léčené skupině nesignifikantně vyšší (49 vs 40 na placebu).
Uvedená studie ukázala dobrý efekt léčby akutního srdečního selhání levosimendanem. Výsledky ukazují příznivý vliv na všechny sledované parametry tak, jak byly prezentovány v kombinovaném cíli. Vyšší mortalita u léčené skupiny může být dána především velikostí souboru a tíží klinického stravu pacientů, dále kombinací s dalšími současně podávanými inotropními a vazodilatačními léky.
Poslední den kongresu v Dallasu byly prezentovány ještě výsledky studie SURVIVE, které jsme dík časnému odletu našeho letadla nestihli a uvedeme je v příštím čísle Kardiologické revue.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2005 Číslo 4
Nejčtenější v tomto čísle
- Akutní infarkt myokardu při okluzi kmene levé věnčité tepny: zkušenosti z počátku 3. tisíciletí
- Plicní hypertenze a cor pulmonale
- Losartan v klinických studiích
- Rehabilitace po infarktu myokardu (III)