Selfmonitoring jako prevence komplikací diabetu
Self‑ monitoring for the prevention of diabetes complications
Over the last few years, not only the number of patients with diabetes, but also the number of patients treated for late complications, has been rapidly increasing. One of the major factors contributing to their development is hyperglycaemia. An important part in preventing the complications is improved diabetes control. Self‑ monitoring plays an irreplaceable role in diabetes treatment. It involves measuring glucose levels and altering therapy according to the measured values. This paper summarizes the latest opinions on use of self‑ monitoring to improve diabetes control in patients with type 1 and type 2 diabetes and provides an overview of the current opportunities for applying technology in diabetology.
Keywords:
diabetes mellitus – late diabetes complications – self‑ monitoring – continuous glucose monitoring
Autoři:
R. Kožnarová
Působiště autorů:
Klinika diabetologie Centra diabetologie, Institut klinické a experimentální medicíny, Praha
Vyšlo v časopise:
Kardiol Rev Int Med 2014, 16(2): 148-151
Kategorie:
Interní medicína
Souhrn
V posledních letech prudce roste nejen počet pacientů s diabetem, ale i počet pacientů léčených pro jeho pozdní komplikace. Jeden ze zásadních faktorů, které se podílejí na jejich vzniku, je hyperglykemie. V prevenci komplikací významně pomáhá zlepšení kompenzace diabetu. Nezastupitelnou součástí léčby diabetu je selfmonitoring (samostatné měření) glykemií a úprava terapie podle naměřených hodnot. Práce shrnuje nejnovější názory na uplatnění selfmonitoringu ve zlepšení kompenzace u pacientů s diabetem 1. i 2. typu a podává přehled současných možností využití technologií v diabetologii.
Klíčová slova:
diabetes mellitus – pozdní komplikace diabetu – selfmonitoring – kontinuální monitorace glykemie
Úvod
V České republice bylo v roce 2012 léčeno 841 227 pacientů s diabetem, což oproti předešlému roku představovalo nárůst prevalence o téměř 16 tisíc diabetiků. Prevalence tohoto onemocnění roste v dlouhodobém trendu, stejně jako roste počet jeho chronických komplikací (obr. 1), které mělo v roce 2012 více než 241 tisíc pacientů [1].
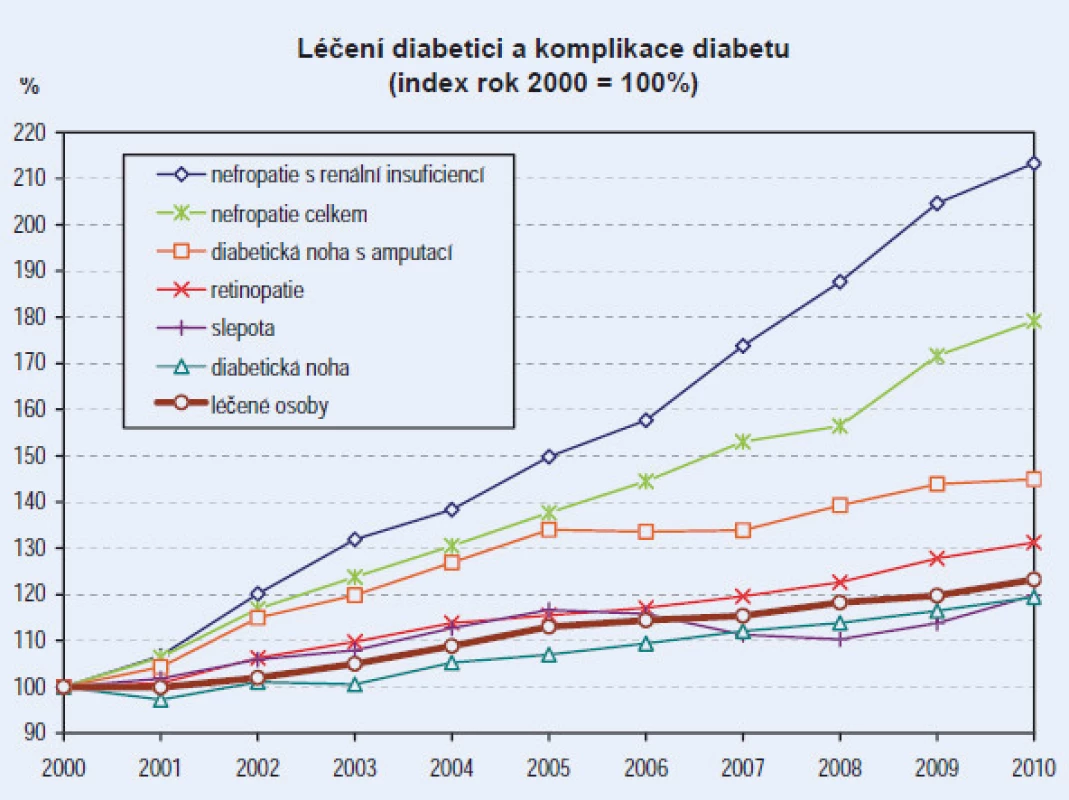
Kompenzace diabetu je důležitým faktorem v prevenci jeho komplikací. Řada studií prokázala, že zvýšené hodnoty glykovaného hemoglobinu (HbA1c) jsou asociovány se zvýšeným rizikem orgánových komplikací jak u diabetu 1. typu, tak 2. typu a že redukce HbA1c toto riziko snižuje.
Znalost glykemie je základním předpokladem pro kvalitní život nemocných s diabetes mellitus. Význam selfmonitoringu je jednoznačný u pacientů s diabetem 1. typu i u pacientů s diabetem 2. typu léčených inzulinoterapií [2]. Názory na význam selfmonitoringu pro pacienty s diabetem 2. typu léčené perorálními antidiabetiky jsou zatím nejednotné. Nicméně pouze na základě znalosti glykemických profilů a jejich změn je pacient schopen správně upravovat dávkování inzulinu. Jak prokazují klinické studie, existuje nepřímá úměra mezi průměrným počtem glykemií změřených během dne a hodnotou HbA1c. Ani velmi dobře spolupracující pacient však nedokáže zachytit všechny oscilace glykemií. Monitorování glykemie je také pro pacienta značným omezením, takže jakékoli jeho usnadnění vede k lepší compliance pacienta. To vše mohou alespoň částečně řešit nové technologie v monitorování glykemií.
Pozdní komplikace diabetu
Asociace kompenzace diabetu a rozvoje jeho orgánových komplikací je více vyjádřena u pacientů s diabetes mellitus 1. typu [3]. U pacientů s diabetem 2. typu je etiopatogeneza komplikací multifaktoriální, ale hyperglykemie zde také hraje významnou roli [4].
Studie UKPDS (United Kingdom Prospective Diabetes Study) [5] demonstrovala význam kompenzace diabetu u pacientů s diabetem 2. typu. Prokázala, že redukce HbA1c o 1 % sníží riziko infarktu myokardu o 14 % a riziko mikrovaskulárních komplikací (diabetická nefropatie, retinopatie a polyneuropatie) o 37 %.
U pacientů s diabetes mellitus 1. typu probíhala dlouhodobá studie, jejíž výsledky bylo možno loni zhodnotit s odstupem 30 let [6]. Studie nesla název DCCT (Diabetes Control and Complications Trial) [7] a její pokračování se nazývá EDIC (Epidemiology of Diabetes Intervention and Complications). Studie DCCT prokázala, že na každých 10 % snížení glykovaného hemoglobinu připadá 44% redukce mikrovaskulárních komplikací diabetu. Studie EDIC prokázala 42% snížení rizika jakékoli kardiovaskulární choroby a 57% snížení rizika nefatálního infarktu myokardu, cévní mozkové příhody a smrti kardiovaskulárního původu.
Metaanalýza Stettlera et al z roku 2006 [8] hodnotila makrovaskulární komplikace. Prokázala, že z lepší kompenzace profitují hlavně pacienti s diabetem 1. typu a mladší pacienti s diabetem s kratším trváním choroby.
Tyto a řada dalších studií vedly k tomu, že je kladen větší důraz na ovlivnění kompenzace diabetu nejen medikamentózní terapií, ale i přístupem ze strany pacienta. Zejména proto, že největší limitací léčby diabetu je vždy hypoglykemie. K tomu pomáhá selfmonitoring (samostatná kontrola) diabetu [9,10].
Selfmonitoring v léčbě diabetu
Selfmonitoring by měl provádět každý pacient s diabetem léčený inzulinem. Pro diabetes 1. typu je dostatek důkazů, že se kompenzace zlepšuje s počtem měření. Maximum zlepšení je mezi 5 a 7 měřeními denně. Selfmonitoring výrazně snižuje riziko hypoglykemie a významně zlepšuje kvalitu života. Doporučení České diabetologické společnosti k provádění selfmonitoringu vycházejí z doporučení evropské a americké diabetologické společnosti:
- a) Pacienti s diabetem léčení konvenčním inzulinovým režimem (1– 2denní dávky inzulinu) – každý den stanovit alespoň 2× glykemii, dále se doporučuje kontrola cukru v moči alespoň 2× týdně před jídlem a 2 hod po jídle.
- b) Pacienti s diabetem léčení intenzifikovaným inzulinovým režimem (tři a více denních dávek inzulinu) – denně profil 3– 4 glykemií nejlépe před jídlem. Nejméně 1× měsíčně by měl pacient zkontrolovat i noční profil (v 1 a 4 hod, popř. pouze ve 3 hod).
- c) Pacienti s diabetem léčení inzulinovou pumpou – denní měření 3– 4 glykemií, nejméně 1× měsíčně i noční profil (v 1 a ve 4 hod, popř. pouze ve 3 hod).
Selfmonitoring u pacientů s diabetem neléčených inzulinem je předmětem diskuze [11,12]. Jeho efektivita je závislá především na schopnosti pacienta reagovat na naměřené hodnoty glykemií a na motivaci zdravotníků naměřené profily s pacientem diskutovat. Na základě metaanalýzy studií selfmonitoringu provedených u pacientů s diabetem 2. typu se doporučuje:
Pravidelné monitorování glykemie před návštěvou lékaře speciálně u pacientů, kteří adekvátně nereagují na naměřené hodnoty glykemie. Např. týden před kontrolou má pacient měřit tzv. velké profily – glykemie před hlavními jídly, za 1– 2 hod po jídle. Jinou možností je měření glykemie alespoň 2× týdně ráno nalačno a 1– 2 hod po jídle.
Technologie využívané k provádění selfmonitoringu
Selfmonitoring s využitím glukometru
Glukometry stále zůstávají nejběžnějším prostředkem k monitoraci glykemie hlavně díky své ceně a jednoduchosti. Současná nabídka glukometrů je velmi široká. Zahrnuje jak přístroje velmi jednoduché, cenově dostupné i pacientům, kteří nemají nárok na úhradu zdravotní pojišťovnou, tak přístroje s řadou doplňkových funkcí, jako je např. elektronický diář, kde pacient může zaznamenávat k naměřené glykemii i pohybovou aktivitu, množství požitých sacharidů a akutní příhody. Nejnovějším trendem jsou glukometry, které lze připojit k tzv. chytrému telefonu nebo tabletu a zde analyzovat výsledky měření či je třeba odesílat ošetřujícímu lékaři. S přílivem nových přístrojů je v poslední době věnována velká pozornost jejich přesnosti. Dle normy ISO 15197 z roku 2012 se musí výsledek naměřený na glukometru pohybovat v rozmezí ± 15 % hodnoty naměřené ze stejného vzorku v laboratoři [13].
Běžnou výbavou glukometru je dnes možnost stanovení hodnoty glykemie z alternativního místa (jinde než na bříšku prstu) [14]. Zajišťuje větší pohodlí pro pacienta a hlavně menší bolestivost odběru, neboť ke stanovení je nutné menší množství krve. To může často vést i k lepší compliance pacienta. U většiny glukometrů představuje alternativní místo vpichu pouze předloktí. U některých glukometrů je možno využít i jiná místa, a to thenar, hypothenar, paži, stehno a lýtko (obr. 2).
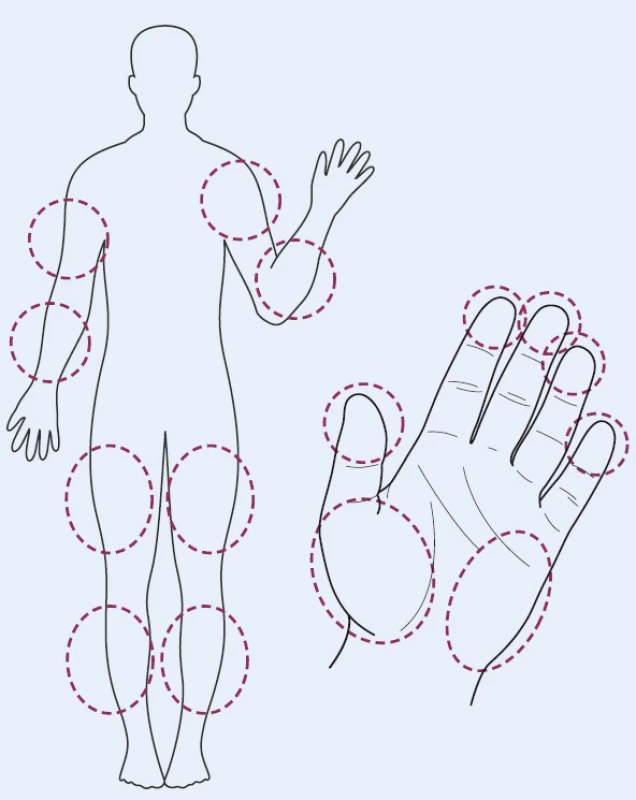
Pro pacienty s poruchou zraku jsou určeny glukometry s hlasovým výstupem. Tyto glukometry zajišťují nezávislost pacienta na pomoci druhé osoby při monitoraci glykemie a jsou běžně k dispozici na našem trhu.
Selfmonitoring s využitím kontinuální monitorace glykemie
Nejnovějším trendem u pacientů s diabetem léčených intenzifikovanými inzulinovými režimy nebo inzulinovou pumpou jsou kontinuální monitory glykemie [15,16]. Kontinuální monitorace glykemií podává maximum informací o jejích výkyvech během dne (obr. 3) a dává pacientům i zdravotníkům možnost optimalizovat léčbu diabetu [17,18]. Správná indikace kontinuální monitorace glykemií je důležitá nejen z hlediska její maximální efektivity pro zlepšení kompenzace diabetu, ale také z hlediska její bezpečnosti a přínosu pro kvalitu života pacienta [19].
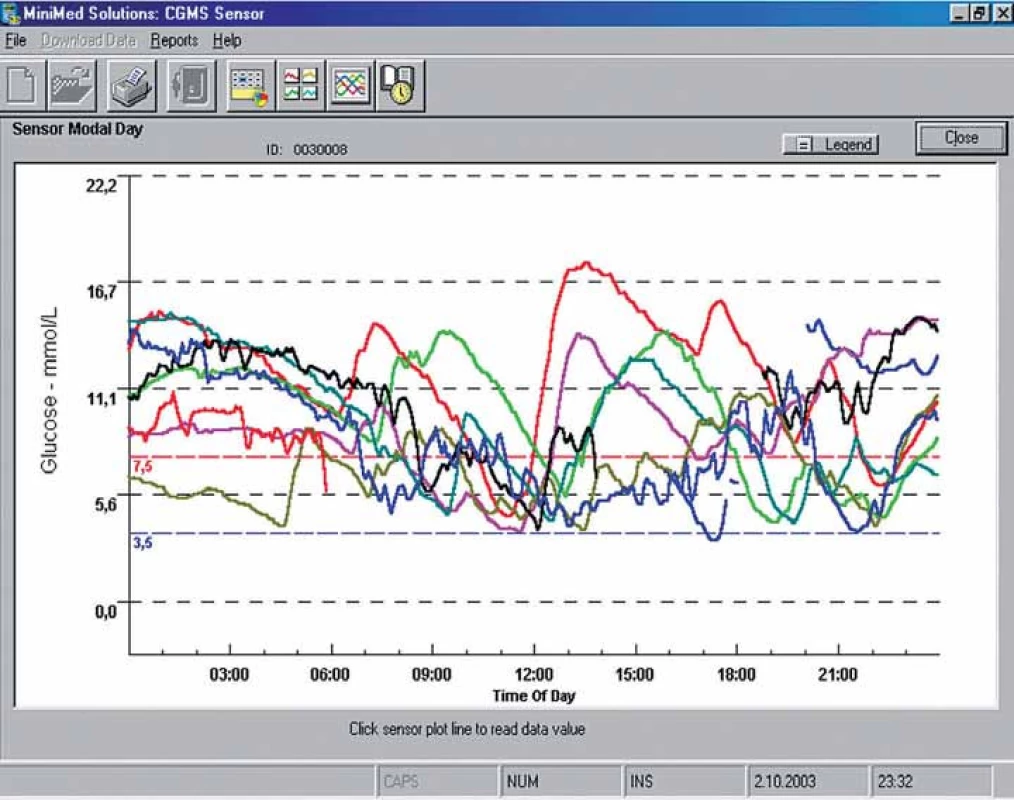
Současné studie svědčí o tom, že pomocí kontinuální monitorace lze dosáhnout zlepšení kompenzace diabetu jak u pacientů s výrazně neuspokojivou kompenzací [20], tak u pacientů s mírně zhoršenou kompenzací [21], u nichž dochází především ke snížení počtu hypoglykemií [22]. Riziko hypoglykemií snižuje především monitorace v reálném čase, při níž může pacient reagovat na alarmy a trendy snižování glykemie i na zjištěnou hypoglykemii [23]. Řada studií ukazuje vysokou frekvenci nerozpoznaných hypoglykemií v průběhu noci [24]. Rozpoznání těžkých hypoglykemií, které mohou způsobit závažné komplikace, je jedním z nejdůležitějších přínosů kontinuální monitorace [25]. V tomto bodě jsou velmi dobrými pomocníky nastavitelné limity pro alarmy a možnost projekce vývoje glykemií, kdy je přístroj na základě vývoje aktuálních glykemií schopen pacienta předem upozornit na zvýšené riziko vzniku hypo‑ i hyperglykemií (obr. 4). Oběma těmito funkcemi jsou vybaveny všechny současné přístroje pro kontinuální monitorování glykemie v reálném čase [26]. Jako optimální využití se v této fázi poznání jeví možnost občasného kontinuálního monitorování u spolupracujících nemocných, převážně s diabetem 1. typu, s hypoglykemiemi či s neuspokojivou kompenzací diabetu. Lze také odhalit a řešit rezervy v dodržování diabetického režimu a diety (možnost vidět a zachytit vzestupy a poklesy glykemií a naučit se adekvátně na ně reagovat). Soustavné monitorování glykemie pomocí senzorů je finančně velmi náročné a využívá jej pouze malé procento pacientů. Obecně však platí, že čím delší čas se stráví monitorováním, tím větší pokles HbA1c lze očekávat. Nejlepších výsledků dosahují pacienti, kteří kontinuální monitoraci využívají ve více než 60 % času [27].
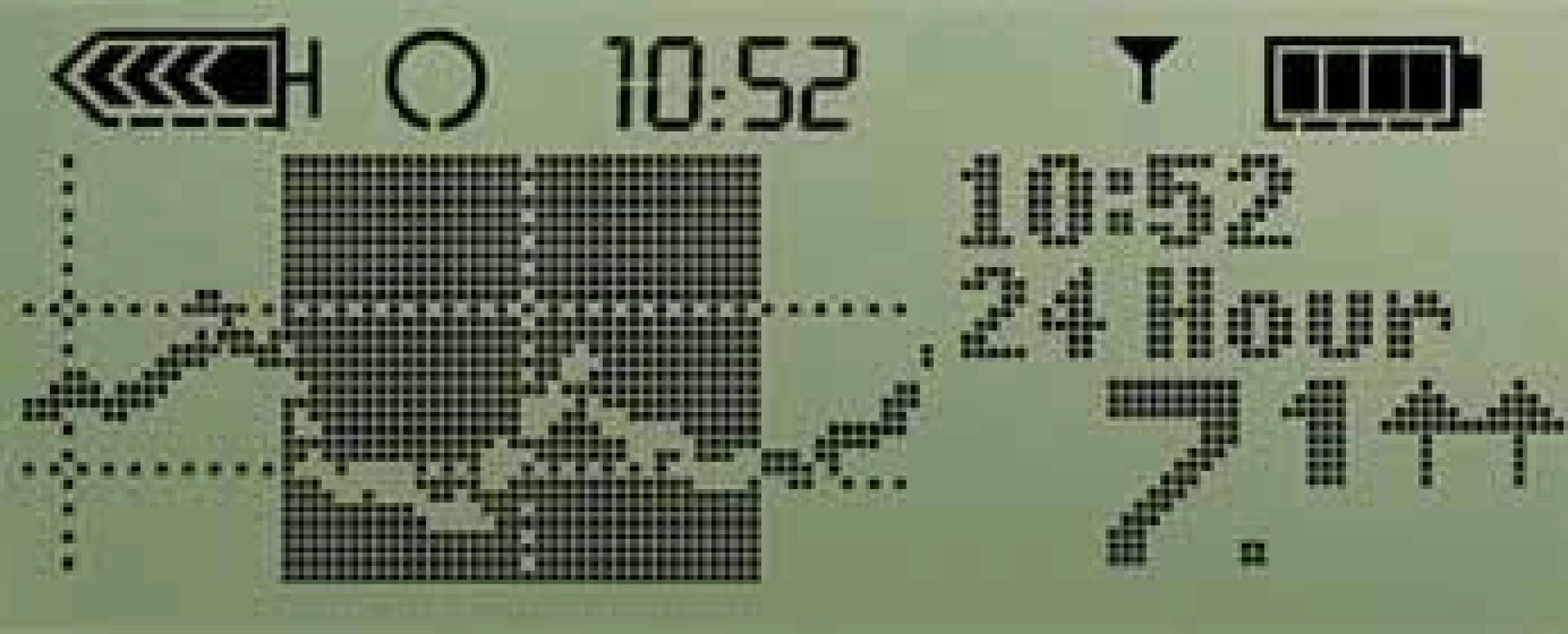
Uzavřený okruh podávání inzulinu
Na výzkum v oblasti kontinuální monitorace glykemie přímo navazuje možnost automatického podávání inzulinu bez zásahu pacienta. Ta by jako jediná zajistila normoglykemii, a tudíž nejlepší prevenci komplikací diabetu. Příkladem takové prevence může být navození normoglykemie u pacientů po úspěšné transplantaci pankreatu, kdy se zastavují či zlepšují mikrovaskulární komplikace diabetu [28].
Již řadu let probíhají různé studie, které se snaží vytvořit tzv. uzavřený okruh podávání inzulinu. Podstatou je kontinuální monitoring glykemie v reálném čase, vyhodnocení výsledku pomocí počítačového algoritmu a následně opět počítačem řízená aplikace inzulinu k udržení normoglykemie. Dostupné systémy zatím dovedou udržet hladinu glykemie v normě během noci, ale s příjmem potravy a pohybem pacienta stávající algoritmy nejsou schopny dosáhnout normoglykemie.
Závěr
Význam selfmonitoringu pro udržení a zlepšení kompenzace diabetu, a tím i prevenci či příznivé ovlivnění komplikací diabetu, je nepopiratelný. Edukace pacienta v selfmonitoringu a samostatných úpravách terapie by měla být nedílnou součástí návštěv pacienta v diabetologické ambulanci. Technologie využívané k selfmonitoringu glykemie zaznamenaly v poslední době sice nebývalý rozmach, ale jejich spolehlivost a hlavně cenová dostupnost jsou zatím limitujícím faktorem jejich praktického použití.
Podpořeno MZ ČR – RVO („Institut klinické a experimentální medicíny – IKEM, IČ 00023001“).
Doručeno do redakce 31. 3. 2014
Přijato po recenzi 8. 4. 2014
MUDr. Radomíra Kožnarová
www.ikem.cz
rakz@medicon.cz
Zdroje
1. Ústav zdravotnických informací a statistiky ČR [online]. Dostupné z: http:/ / www.uzis.cz
2. Cohen N, Shaw JE. Diabetes: advances in treatment. Intern Med J 2007; 37: 383– 388.
3. Kilpatrick ES, Rigby AS, Atkin SL. The effect of glucose variability on the long‑term risk of microvascular complications in type 1 diabetes. Diabetes Care 2006; 29: 1468– 1490.
4. Prázný M. Mikroangiopatie a diabetes mellitus. In: Perušičová J, Češka R et al (eds). KARDIABETES. Kardiovaskulární choroby a diabetes mellitus. Brno: Facta Medica 2009: 35– 47.
5. UK Prospective Diabetes Study Group. Intensive blood‑ glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patiens with type 2 diabetes (UKPDS 33). Lancet 1998; 352: 837– 853.
6. Gubitosi‑ Klug RA, DCCT/ EDIC Research Group. The diabetes control and complications trial/ epidemiology of diabetes interventions and complications study at 30 years: Summary and future directions. Diabetes Care 2014; 37; 44– 49. doi: 10.2337/ dc13– 2148.
7. The Diabetes Control and Complications Trial Group. The effect of intensive treatment of diabetes on development and progression of long‑term complications in insulin-dependent diabetes mellitus. N Engl J Med 1993; 329: 977– 986.
8. Stettler C, Allemann S, Jüni P et al. Glycaemic control and macrovascular disease in types 1 and 2 diabetes mellitus: Meta‑analysis of randomised trials. Am Heart J 2006; 152: 27– 38.
9. Janíčková‑ Žďárská D. Glykovaný hemoglobin a selfmonitoring glykemie – jejich využití a limitace. In: Kvapil M (ed). Diabetologie 2010. Praha: Triton 2010: 117– 131.
10. Mc Andrew L, Schneider SH, Burns E et al. Does patient blood glucose monitoring improve diabetes control? A systematic rewiew of the literature. Diabetes Educ 2007; 33: 991– 1011.
11. Martin S, Schneider B, Heinemann L et al. Self‑ monitoring of blood glucose in type 2 diabetes and long‑term outcome: an epidemiological cohort study. Diabetologia 2006; 49: 271– 278.
12. Welschen LM. Bloemendal E, Nijpels et al. Self‑ monitoring of blood glucose in patiens with type 2 diabetes who are not using insulin: a systematic rewiew. Diabetes Care 2005; 28: 1510– 1517.
13. Freckmann G, Schmid C, Baumstark A et al. System accuracy evaluation of 43 blood glucose monitoring systems for self‑ monitoring of blood glucose according to DIN EN ISO 15197. J Diabetes Sci Technol 2012; 6: 1060– 1075.
14. Fineberg SE, Bergenstal RM, Bernstein RM et al. Use of an automatic device for alternative site blood glucose monitoring. Diabetes Care 2001; 24: 1217– 1220.
15. JDRF Continuous Glucose Monitoring Study Group, Tamborlane WV, Beck RW, Bode BW et al. Continuous glucose monitoring and intensive treatment of type 1 diabetes. N Engl J Med 2008; 359: 1464– 1476. doi: 10.1056/ NEJMoa0805017.
16. Joubert M, Reznik Y. Personal continuous glucose monitoring (CGM) in diabetes management: rewiew of the litrature and implementation for practical use. Diabetes Res Clin Pract 2012; 96: 294– 305. doi: 10.1016/ j.diabres.2011.12.010.
17. Brož J. Kontinuální monitoring glykémie: přehled přístrojů, indikace, efektivita a přesnost metody. In: Rušavý Z et al (ed). Technologie v diabetologii. Praha: Galén 2010: 142– 152.
18. Kožnarová R. Novinky v monitoraci glykemie. Remedia 2012; 22: 72– 76.
19. Jirkovská A. Základní zásady kontinuální monitorace glykemie – pomohou nám v kompenzaci diabetu? Kazuistiky v diabetologii 2011; 4: 4– 8.
20. Deiss D, Bolinder J, Riveline JP et al. Improved glycemic control in poorly controlled patients with type 1 diabetes using real‑ time continuous glucose monitoring. Diabetes Care 2006; 29: 2730– 2732.
21. Garg S, Zisser H, Schwartz S et al. Improvement in glycaemic excursions with a transcutaneous, real‑ time continuous glucose sensor: a randomized controlled trial. Diabetes Care 2006; 29: 44– 50.
22. Bailey TS, Zisser HC, Garg SK. Reduction in hemoglobin A1C with real‑ time continuous glucose monitoring: results from a 12‑week observational study. Diabetes Technol Ther 2007; 9: 203– 210.
23. Maia FF, Araújo LR. Efficacy of continuous glucose monitoring system (CGMS) to detect postprandial hyperglycemia and unrecognized hypoglycemia in type 1 diabetic patients. Diabetes Res Clin Pract 2007; 75: 30– 34.
24. Wentholt IM, Maran A, Masurel N et al. Nocturnal hypoglycaemia in Type 1 diabetic patients, assessed with continuous glucose monitoring: frequency, duration and associations. Diabet Med 2007; 24: 527– 532.
25. Battelino T, Philip M, Bratina N et al. Effect of continuous glucose monitoring on hypoglycaemia in type 1 diabetes. Diabetes Care 2011; 34: 795– 800. doi: 10.2337/ dc10– 1989.
26. Bode B, Gross K, Rikalo N et al. Alarms based on real‑ time sensor glucose values alert patients to hypo‑ and hyperglycaemia: the guardian continuous monitoring system. Diabetes Technol Ther 2004; 6: 105– 113.
27. Gilliam LK, Hirsch IB. Practical aspects of real‑ time continuous glucose monitoring. Diabetes Technol Ther 2009; 11 (Suppl 1): S75– S82. doi: 10.1089/ dia.2008.0135.
28. Kožnarová R, Saudek F, Sosna T et al. Beneficial effect of pancreas and kidney transplantation on advanced diabetic retinopathy. Cell Transplant 2000; 9: 903– 908.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2014 Číslo 2
Nejčtenější v tomto čísle
- Centrálně působící antihypertenziva – rilmenidin
- Mechanická podpora oběhu v léčbě kardiogenního šoku – přehled
- Mechanické podpory a transplantace srdce v léčbě chronického srdečního selhání
- Nefarmakologická léčba srdečního selhání z pohledu nových evropských doporučení pro srdeční resynchronizační léčbu
